
分析 (1)要配制450mL 0.2mol•L-1FeSO4溶液,應選擇500mL容量瓶,實際配制500mL溶液,依據m=CVM計算需要綠礬的質量;
(2)依據配制一定物質的量濃度溶液的一般步驟排序;
(3)分析操作對溶質的物質的量和溶液的體積,依據C=$\frac{n}{V}$進行誤差分析;
(4)高錳酸鉀與二價鐵離子反應,紫色的高錳酸根離子被還原為無色的二價錳離子.
解答 解:(1)要配制450mL 0.2mol•L-1FeSO4溶液,應選擇500mL容量瓶,實際配制500mL溶液,需要溶質的質量m=0.2mol/L×0.5L×278g/mol=27.8g;
故答案為:27.8;
(2)配制一定物質的量濃度溶液的一般步驟:計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻、裝瓶,所以正確的操作為:①②④③⑤;
故答案為:①②④③⑤;
(3)A.若配制時遺漏步驟④,導致溶質的物質的量偏小,溶液濃度偏低,不A不選;
B.定容時俯視刻度線,導致溶液體積偏小,溶液濃度偏高,故B選;
C.依據左盤質量=右盤質量+游碼質量,所以稱量時物、碼放反了,實際稱量的固體為27-0.8=26.2g,溶質的物質的量偏小,溶液濃度偏低,故C不選;
D.綠礬樣品已部分風化,27.8g固體中含有的溶質的物質的量偏大,溶液濃度偏高,故D選;
E.搖勻后溶液低于刻度線,再加入蒸餾水使液面最低點與刻度線相切,導致溶液體積偏大,溶液濃度偏低,故E不選;
F.玻璃棒在刻度線上方引流水,則易造成刻度線上方水有粘留,故定容完成后溶液體積會偏大,濃度會偏小,故F不選;
故選:D;
(4)高錳酸鉀與二價鐵離子反應,紫色的高錳酸根離子被還原為無色的二價錳離子,溶液顏色變為無色或者變淺,所以不需要加入指示劑;
故答案為:不需要;高錳酸鉀有很深的紫色,滴定中體現氧化性,被還原后紫色消失或變淺.
點評 本題考查了一定物質的量濃度溶液的配制,明確配制原理和過程是解題關鍵,注意容量瓶、量筒規格選擇的依據,注意誤差分析的方法和技巧,題目難度不大.


 中考解讀考點精練系列答案
中考解讀考點精練系列答案科目:高中化學 來源: 題型:解答題
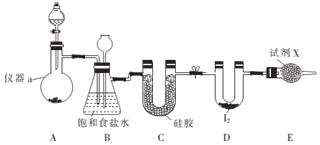
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
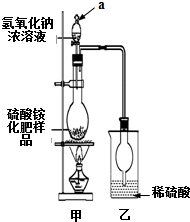 硫酸銨是一種常用的銨態氮肥.國家規定的質量標準如下:
硫酸銨是一種常用的銨態氮肥.國家規定的質量標準如下:| 指標 項目 | 優等品 | 一等品 | 合格品 |
| 外 觀 | 白色結晶,無可見機械雜質 | 無可見機械雜質 | |
| 氮(N)含量 | ≥21.0% | ≥21.0% | ≥20.5% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | -317.3kJ/mol | B. | +317.3 kJ/mol | C. | -379.3kJ/mol | D. | -332.8kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
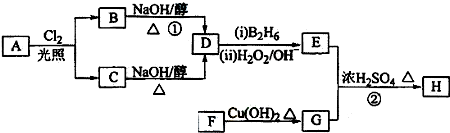
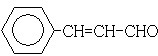 ;
;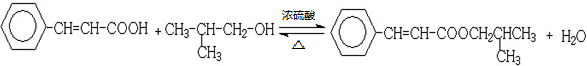 ;
; 、
、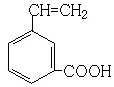 、
、 、
、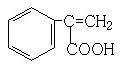 (其中任意兩種).
(其中任意兩種).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 適量攝入油脂,有助于人體吸收多種脂溶性維生素和胡蘿卜素 | |
| B. | 利用油脂在堿性條件下的水解,可以生產甘油和肥皂 | |
| C. | 植物油通過氫化可以制造植物奶油(人造奶油) | |
| D. | 脂肪是有機體組織里儲存能量的重要物質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使酚酞呈紅色的溶液:Na+、NH4+、Al3+、NO3- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=0.1mol•L-1的溶液:Na+、K+、CO32-、ClO- | |
| C. | 含有Fe3+的溶液:Na+、Al3+、Cl-、SCN- | |
| D. | 由水電離產生的c(OH-)=1×10-14mol•L-1溶液:K+、Na+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
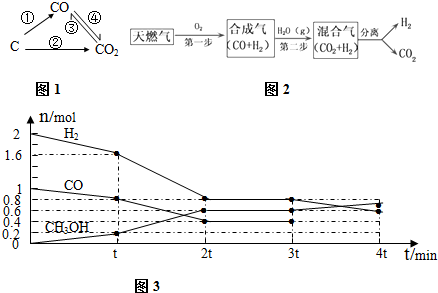
| 容器編號 | c(CO)/mol.L-1 | c(O2)/mol.L-1 | (CO2)/mol.L-1 | v(正)和v(逆)比較 |
| Ⅰ | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | v(正)>v(逆) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com