

 .
.分析 (1)依據(jù)熱化學方程式和蓋斯定律計算分析;
(2)反應(yīng)Ⅱ吸熱反應(yīng),依據(jù)反應(yīng)自發(fā)進行的判斷依據(jù)是△H-T△S<0分析;
(3)①不同水碳比$\frac{n({H}_{2}O)}{n(C{O}_{2})}$和溫度影響CO2平衡轉(zhuǎn)化率變化的趨勢曲線分析可知,
②反應(yīng)Ⅲ是放熱反應(yīng),升溫平衡逆向進行;
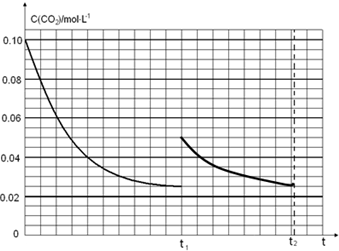
(4)圖象分析二氧化碳的平衡濃度為0.025mol/L,體積縮小一半濃度增大一倍應(yīng)為0.05mol/L,隨反應(yīng)進行達到平衡狀態(tài),因為生成物為固體,最后達到相同平衡狀態(tài),二氧化碳濃度不變,據(jù)此畫出變化曲線;
(5)分析尿素結(jié)構(gòu)可知,和羰基連接的氨基據(jù)此性質(zhì)分析推斷.
解答 解:(1)反應(yīng)Ⅰ:2NH3(g)+CO2(g)?NH2CO2NH4(s)△H1=a kJ•mol-1
反應(yīng)Ⅱ:NH2CO2NH4(s)?CO(NH2)2(s)+H2O(g)△H2=+72.49kJ•mol-1
總反應(yīng)Ⅲ:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)△H3=-86.98kJ•mol-1
由蓋斯定律總反應(yīng)Ⅲ-反應(yīng)Ⅱ,得到2NH3(g)+CO2(g)?NH2CO2NH4(s)△H1=a=-159.47kJ•mol-1,
故答案為:-159.47 kJ•mol-1;
(2)反應(yīng)Ⅱ:NH2CO2NH4(s)?CO(NH2)2(s)+H2O(g)△H2=+72.49kJ•mol-1,反應(yīng)前后氣體體積增大,△S>0,焓變分析可知是吸熱反應(yīng),△H>0,所以依據(jù)反應(yīng)自發(fā)進行的判斷依據(jù)△H-T△S<0,需要在高溫下反應(yīng)自發(fā)進行,
故答案為:>;高溫;
(3)①反應(yīng)Ⅲ:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)△H3=-86.98kJ•mol-1,其他條件相同時,為提高CO2的平衡轉(zhuǎn)化率,平衡正向進行,依據(jù)圖象中的水碳比數(shù)據(jù)分析判斷,生產(chǎn)中可以采取的措施是降低水碳比,二氧化碳轉(zhuǎn)化率增大,
故答案為:降低;
②反應(yīng)Ⅲ:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)△H3=-86.98kJ•mol-1,是放熱反應(yīng),升溫高于190°C,依據(jù)圖象分析可知,二氧化碳轉(zhuǎn)化率減小,因為溫度升高,平衡逆向進行,
故答案為:溫度高于190℃時,因為反應(yīng)Ⅲ是放熱反應(yīng),溫度升高平衡向逆方向進行,CO2的平衡轉(zhuǎn)化率降低;
(4)在恒溫下將0.4mol NH3和0.2mol CO2放入容積為2L的密閉容器中,達到平衡時,
2NH3(g)+CO2(g)?NH2CO2NH4(s)
起始量(mol/L) 0.2 0.1 0
變化量(mol/L) 0.15 0.075
平衡量(mol/L) 0.05 0.025
t1時達到平衡過程中c(CO2)隨時間t變化趨勢曲線如圖2所示.若其他條件不變,t1時將容器體積壓縮到1L,二氧化碳濃度應(yīng)增大到0.05mol/L,壓強增大,平衡正向進行,由于生成物是固體,所以達到平衡狀態(tài),二氧化碳濃度保持不變,據(jù)此畫出變化曲線為: ,
,
故答案為: ;
;
(5)尿素在土壤中會發(fā)生反應(yīng)CO(NH2)2+2H2O?(NH4)2CO3.分析結(jié)構(gòu)特征可知,物質(zhì)性質(zhì)取決于官能團,尿素中氨基和羰基相連,能夠與水反應(yīng)生成銨根離子,所以選項中符合此結(jié)果特征的有類似性質(zhì),
A.NH2COONH4 ,結(jié)構(gòu)中含有與羰基連接的氨基,故A符合;
B.H2NOCCH2CH2CONH2 結(jié)構(gòu)中含有與羰基連接的氨基,故B符合;
C.HOCH2CH2OH,結(jié)構(gòu)中不含有氨基,故C不符合;
D.HOCH2CH2NH2,分子中的氨基不是和羰基連接,不具有此性質(zhì),故D不符合;
故答案為:AB.
點評 本題考查較為綜合,涉及熱化學方程式和蓋斯定律的計算應(yīng)用、化學平衡影響因素分析判斷、平衡常數(shù),圖象繪制與分析等知識,題目難度較大,明確化學平衡及其影響為解答關(guān)鍵,注意掌握蓋斯定律的內(nèi)容及應(yīng)用,試題培養(yǎng)了學生的靈活應(yīng)用能力.


 名題金卷系列答案
名題金卷系列答案科目:高中化學 來源: 題型:選擇題
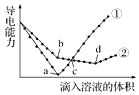 在兩份相同的Ba(OH)2溶液中,分別滴入物質(zhì)的量濃度相等的H2SO4、NaHSO4溶液,其導電能力隨滴入溶液體積變化的曲線如圖所示.下列分析不正確的是( )
在兩份相同的Ba(OH)2溶液中,分別滴入物質(zhì)的量濃度相等的H2SO4、NaHSO4溶液,其導電能力隨滴入溶液體積變化的曲線如圖所示.下列分析不正確的是( )| A. | c點,兩溶液中含有相同量的OH- | |
| B. | b點,溶液中大量存在的離子是Na+、OH- | |
| C. | ①代表滴加H2SO4溶液的變化曲線 | |
| D. | a、d兩點對應(yīng)的溶液均顯中性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在加入鋁粉能產(chǎn)生氫氣的溶液中:Fe2+、K+、NO3-、Cl- | |
| B. | 澄清透明的溶液:Cu2+、SO42-、Mg2+、Cl- | |
| C. | 含有大量Al3+的溶液中:K+、Ba2+、AlO2-、Cl- | |
| D. | pH=1的溶液:Na+、ClO-、K+、CH3COO- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4NO3化肥結(jié)塊后可以用木棒敲擊砸碎后再使用 | |
| B. | 染發(fā)劑有植物染發(fā)劑、無機染發(fā)劑、合成染發(fā)劑等 | |
| C. | 常用洗滌劑的主要成分是表面活性劑 | |
| D. | 有機磷農(nóng)藥比有機氯農(nóng)藥易分解,在環(huán)境中殘留時間短 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 開始時左右兩室分子數(shù)相同 | B. | 最終容器內(nèi)無H2存在 | ||
| C. | 反應(yīng)前后H2室壓強相同 | D. | 最終容器內(nèi)密度與原來相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com