
已知25 ℃時,幾種弱酸的電離常數如下:
弱酸的化學式 | CH3COOH | HCN | H2S |
電離常數 | 1.8×10-5 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
25 ℃時,下列說法正確的是( )
A.等物質的量濃度的各溶液pH關系為:pH(Na2S)>pH(NaCN) >pH(NaHS)>pH(CH3COONa)
B.用0.1mol/L的NaOH溶液滴定pH值相等的CH3COOH和HCN溶液,CH3COOH消耗的NaOH溶液體積更大
C.NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)+c(H2S)
D.某濃度的NaCN溶液的pH=d,則其中由水電離出的c(OH-)=10-d mol/L
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2015-2016學年寧夏銀川二中高二下期中化學試卷(解析版) 題型:選擇題
某有機物,當它含有下列的一種官能團時,既能發生取代反應、氧化反應、酯化反應,又能發生消去反應的是( )

查看答案和解析>>
科目:高中化學 來源:2015-2016學年江西吉安一中高二下第二次段考化學試卷(解析版) 題型:選擇題
下列關于有機物的說法中,不正確的是
A.糖類、有脂和蛋白質都能發生水解反應
B.乙烯、氯乙烯均可用于合成塑料
C.甲烷、苯、乙醇和乙酸在一定條件下都能發生取代反應
D.分子式為C6H14的有機物只有5種,它們屬于同分異構體
查看答案和解析>>
科目:高中化學 來源:2015-2016學年重慶市高二下期中化學試卷(解析版) 題型:選擇題
下列化學用語的表達正確的是
A.二氧化碳的比例模型:
B.原子核內有10個中子的氧原子: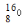
C.Fe3+的最外層電子排布式為3s23p63d5
D.Cu基態的外圍電子排布圖: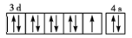
查看答案和解析>>
科目:高中化學 來源:2016屆遼寧省高三下第四次模擬理綜化學試卷(解析版) 題型:填空題
【化學---選修3:物質結構與性質】原子序數小于36的X、Y、Z、W四種元素,其中X是半徑最小的元素,Y原子基態時最外層電子數是其內層電子總數的2倍,Z原子基態時2p原子軌道上有3個未成對的電子,W原子4s原子軌道上有1個電子,M能層為全充滿的飽和結構。回答下列問題:

(1)W基態原子的價電子排布式____________;Y2X2分子中Y原子軌道的雜化類型為______。
(2)化合物ZX3的沸點比化合物YX4的高,其主要原因是_____________。
(3)元素Y的一種氧化物與元素Z的一種氧化物互為等電子體,元素Z的這種氧化物的分子式是____________。Y60用做比金屬及其合金更為有效的新型吸氫材料,其分子結構為球形32面體,它是由60個Y原子以20個六元環和12個五元環連接而成的具有30個Y=Y鍵的足球狀空心對稱分子。則該分子中σ鍵和π鍵的個數比_____;36gY60最多可以吸收標準狀況下的氫氣_____L。
(4)元素W的一種氯化物晶體的晶胞結構如右圖所示,該氯化物的化學式是___________,該晶體中W的配位數為___________。它可與濃鹽酸發生非氧化還原反應,生成配合物HnWCl3,反應的化學方程式為_________。
查看答案和解析>>
科目:高中化學 來源:2016屆遼寧省高三下第四次模擬理綜化學試卷(解析版) 題型:選擇題
依據下列實驗現象,得出的結論正確的是 ( )
選項 | 操作 | 實驗現象 | 結論 |
A | 向NaBr溶液中加入氯水,再加入淀粉?KI溶液 | 溶液變藍 | 氧化性:Cl2>Br2>I2 |
B | 將鋁片放入鹽酸中 | 產生氣泡的速率開始較慢,隨后加快,后來又逐漸減慢 | H+的濃度是影響反應速率的唯一因素 |
C | 向蔗糖溶液中加入稀硫酸,水浴加熱后,加入新制氫氧化銅懸濁液,加熱 | 得到藍色溶液 | 蔗糖水解產物沒有還原性或蔗糖未水解 |
D | 向漂白粉中滴入稀硫酸,將生成的氣體通入品紅溶液 | 品紅溶液褪色 | 氣體中含有Cl2 |
查看答案和解析>>
科目:高中化學 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:實驗題
苯胺為無色液體,還原性強,易被氧化;有堿性,與酸反應生成鹽。常用硝基苯與H2制備: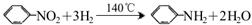 。
。
其部分裝置及有關數據如下:
沸點/℃ | 密度g/mL | 溶解性 | |
硝基苯 | 210.9 | 1.20 | 不溶于水,易溶于乙醇、乙醚 |
苯胺 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚 |
乙醚 | 34.6 | 0.71 | 不溶于水,易溶于硝基苯、苯胺 |
實驗步驟:
①檢查裝置的氣密性,連接好C處冷凝裝置的冷水。
②先向三頸燒瓶中加入沸石及硝基苯,再取下恒壓分液漏斗,換上溫度計。
③打開裝置A、B間活塞,通入H2一段時間。
④點燃B處的酒精燈,加熱,使溫度維持在140℃進行反應。
⑤反應結束后,關閉裝置A、B間活塞,加入生石灰。
⑥調整好溫度計的位置,繼續加熱,收集182~186℃餾分,得到較純苯胺。
回答下列問題:
(1)步驟⑥中溫度計水銀球的位置在__________。
(2)下列關于實驗的敘述中,錯誤的是__________。
A.冷凝管的冷水應該從b進從a出
B.實驗開始酎,溫度計水銀球應插入反應液中,便于控制反應液的溫度
C.裝置A中應使用鋅粉,有利于加快生成H2的速率
D.加入沸石的目的是防止暴沸
(3)若實驗中步驟③和④的順序顛倒,則實驗中可能產生的后果是_____________。
(4)蒸餾前,步驟⑤中加入生石灰的作用是____________________。
(5)有學生質疑反應完成后,直接蒸餾得到苯胺的純度不高,提出以下流程:

苯胺在酸性條件下生成鹽酸苯胺被水萃取,在堿性溶液中又被放有機溶劑反萃取,這種萃取——反萃取法簡稱反萃。實驗中反萃的作用是__________;在分液漏斗中進行萃取分液時,應注意不時放氣,其目的是____________________。
(6)苯胺還原性強,易被氧化,請配平下列化學方程式的化學計量數。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com