


科目:高中化學 來源: 題型:閱讀理解
 (2010?西城區一模)過氧化氫對環境友好,性質多樣,有很重要的研究和應用價值.
(2010?西城區一模)過氧化氫對環境友好,性質多樣,有很重要的研究和應用價值.
| ||
| 序號 | 條件 | 現象 | 結論 | |
| 溫度/℃ | 催化劑 | |||
| 1 | 40 | FeCl3溶液 | ||
| 2 | 20 | FeCl3溶液 | ||
| 3 | 20 | MnO2 | ||
| 4 | 20 | 無 | ||
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

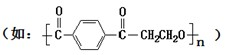 做成,在該類材料做成的容器中混合NH4HCO3固體、H2SiF6濃溶液和H2O時,加入試劑的順序應是
做成,在該類材料做成的容器中混合NH4HCO3固體、H2SiF6濃溶液和H2O時,加入試劑的順序應是查看答案和解析>>
科目:高中化學 來源: 題型:
A.強電解質溶液的導電能力一定比弱電解質溶液的導電能力強
B.因為醋酸是弱電解質,鹽酸是強電解質,所以中和等體積等物質的量濃度的醋酸和鹽酸時,中和醋酸消耗的NaOH比鹽酸消耗的NaOH用量少
C.足量Zn分別和等體積、等物質的量濃度的鹽酸和醋酸反應時,產生H2的量相同,放出H2的速率不等
D.物質的量濃度相同的磷酸鈉溶液和磷酸溶液中![]() 的物質的量濃度相同
的物質的量濃度相同
查看答案和解析>>
科目:高中化學 來源: 題型:
(14分)過氧化氫對環境友好,性質多樣,有很重要的研究和應用價值。
(1)實驗室利用反應可制備氧氣。
①取等物質的量濃度等體積溶液分別進行下列實驗,研究外界條件對該反應速率的影響,實驗報告如下表所示。
| 序號 | 條件 | 現象 | 結論 | |
| 1 | 溫度/℃ | 催化劑 | ||
| 2 | 40 | FeCl3溶液 |
|
|
| 3 | 20 | FeCl3溶液 |
|
|
| 4 | 20 | MnO2 |
|
|
| 5 | 20 | 無 |
|
|
實驗1、2研究的是 對H2O2分解速率的影響。
實驗2、3的目的是 。
實驗中可以表明該反應速率差異的現象是 。
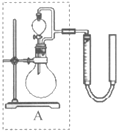
②實驗室用MnO2做該反應的催化劑,使用如右圖所示裝置的A部分制備O2,避免反應過于劇烈的操作是 。
(2)Na2O2與水反應也可生成O2。某同學取4 g Na2O2樣品與過量水反應,待反應完全終止時,得100 mL溶液X和448 mL O2(已折算為標準狀況)。該同學推測樣品中含有雜質或反應中生成H2O2,并進行實驗研究。
①取少量X于試管中,滴加FeCl2溶液,立即生成紅褐色沉淀。則反應的離子方程式是 。
②通過如上圖所示整套實驗裝置測定Na2O2樣品的純度,假設所含雜質不參加反應。取25 mL X,滴入燒瓶內使其與過量KMnO4酸性溶液反應,最終生成56 mL O2(已折算為標準狀況),則此樣品中:Na2O2的質量分數是 。
查看答案和解析>>
科目:高中化學 來源:北京市西城區2010年高三一模(理科綜合)化學部分 題型:實驗題
(14分)過氧化氫對環境友好,性質多樣,有很重要的研究和應用價值。
(1)實驗室利用反應 可制備氧氣。
可制備氧氣。
①取等物質的量濃度等體積 溶液分別進行下列實驗,研究外界條件對該反應速率的影響,實驗報告如下表所示。
溶液分別進行下列實驗,研究外界條件對該反應速率的影響,實驗報告如下表所示。
|
序號 |
條件 |
現象 |
結論 |
|
|
1 |
溫度/℃ |
催化劑 |
||
|
2 |
40 |
FeCl3溶液 |
|
|
|
3 |
20 |
FeCl3溶液 |
|
|
|
4 |
20 |
MnO2 |
|
|
|
5 |
20 |
無 |
|
|
實驗1、2研究的是 對H2O2分解速率的影響。
實驗2、3的目的是 。
實驗中可以表明該反應速率差異的現象是 。
②實驗室用MnO2做該反應的催化劑,使用如右圖所示裝置的A部分制備O2,避免反應過于劇烈的操作是 。

(2)Na2O2與水反應也可生成O2。某同學取4 g Na2O2樣品與過量水反應,待反應完全終止時,得100 mL溶液X和448 mL O2(已折算為標準狀況)。該同學推測樣品中含有雜質或反應中生成H2O2,并進行實驗研究。
①取少量X于試管中,滴加FeCl2溶液,立即生成紅褐色沉淀。則反應的離子方程式是 。
②通過如上圖所示整套實驗裝置測定Na2O2樣品的純度,假設所含雜質不參加反應。取25 mL X,滴入燒瓶內使其與過量KMnO4酸性溶液反應,最終生成56 mL O2(已折算為標準狀況),則此樣品中:Na2O2的質量分數是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com