(2010?西城區一模)甲、乙、丙、丁是由短周期元素組成的物質,它們之間存在如下轉化關系.甲+乙→丙+丁
(1)轉化關系中所涉及的反應為非氧化還原反應,且乙為水.
①若甲為塊狀固體,丙為可燃性氣體,其分子內既含有極性鍵又含有非極性鍵.則丙的電子式是
.
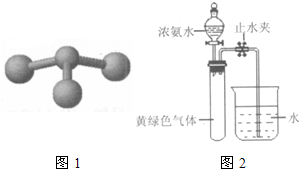
②若甲是由N和Cl元素組成的化合物,其分子結構模型
如圖1所示,丙具有漂白性.則甲中Cl元素的化合價是
+1
+1
.
(2)轉化關系中所涉及的反應為氧化還原反應,且乙為水.
①若甲和丙是同主族元素組成的單質,且組成甲的元素位于第三周期,此反應的離子方程式是
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
.
②若丙和丁都可在一定條件下還原CuO,此反應的化學方程式是
.
③若甲是由N和O元素組成的氣態物質,呈紅棕色.將3.36g Fe加到一定量丙溶液中,收集到1.12L氣體丁(已折算為標準狀況),則反應的離子方程式是
6Fe+20HNO3=3Fe(NO3)2+3Fe(NO3)3+5NO+10H2O
6Fe+20HNO3=3Fe(NO3)2+3Fe(NO3)3+5NO+10H2O
.
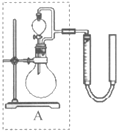
(3)Hofmann依據上述轉化關系測定氨分子的組成.現用如圖2所示的裝置進行實驗,打開分液漏斗的活塞,滴下濃氨水,至不再反應為止;關閉分液漏斗的活塞,待恢復到室溫,打開止水夾,試管內液面上升至
處.
①滴下濃氨水一段時間后,試管內發生反應的化學方程式是
8NH3+3C12=N2+6NH4Cl
8NH3+3C12=N2+6NH4Cl
.
②證明試管內“不再反應”的實驗操作和現象是
待產生的大量白煙沉降后,繼續滴加濃氨水,不再產生白煙
待產生的大量白煙沉降后,繼續滴加濃氨水,不再產生白煙
.

 (2010?西城區一模)過氧化氫對環境友好,性質多樣,有很重要的研究和應用價值.
(2010?西城區一模)過氧化氫對環境友好,性質多樣,有很重要的研究和應用價值.

 (2010?西城區一模)甲、乙、丙、丁是由短周期元素組成的物質,它們之間存在如下轉化關系.甲+乙→丙+丁
(2010?西城區一模)甲、乙、丙、丁是由短周期元素組成的物質,它們之間存在如下轉化關系.甲+乙→丙+丁






 (R、R'代表烴基或氫原子)
(R、R'代表烴基或氫原子)






 )的合成路線:
)的合成路線:


