
分析 ①銅片的稀鹽酸中加入H2O2后,銅片溶解,發生氧化還原反應生成氯化銅、水,該反應中轉移2e-;
②0.06 mol I-→0.02 mol I2+0.02 IO3-轉移0.16 mol電子,由電子守恒計算參加反應的n(KMnO4);
③先由棕黃色變為淺綠色,過一會又變為棕黃色,則Fe3+先被還原后又氧化.
解答 解:①浸泡銅片的稀鹽酸中加入H2O2后,銅片溶解,發生氧化還原反應生成氯化銅、水,反應的化學方程式為,故答案為:Cu+2HCl+H2O2=CuCl2+2H2O;
②0.06 mol I-→0.02 mol I2+0.02 IO3-轉移0.16 mol電子,從MnO4-→Mn2+可以看出,化合價由+7價降低為+2價,由電子守恒可知參加反應的n(KMnO4)=$\frac{0.16mol}{(7-2)}$=0.032 mol,故答案為:0.032;
③先由棕黃色變為淺綠色,過一會又變為棕黃色,則Fe3+先被還原后又氧化,先變為淺綠色的離子方程式是2Fe3++SO32-+H2O=2Fe2++SO42-+2H+,后變為棕黃色的原因是H+與NO3-組成的硝酸將Fe2+氧化,故答案為:2Fe3++SO32-+H2O=2Fe2++SO42-+2H+.
點評 本題考查氧化還原反應,為高頻考點,把握反應中元素的化合價變化為解答的關鍵,側重氧化還原反應基本概念及分析應用能力的考查,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
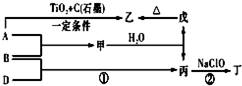 已知 A、B、D為中學常見的單質,甲、乙、丙、丁、戊為短周期元素組成的化合物.其中,丙是一種能使濕潤的紅色石蕊試紙變藍的無色氣體;丁是一種高能燃料,其組成元素與丙相同,1mol 丁分子中不同原子的數目比為1:2,且含有18mol電子;戊是一種難溶于水的白色膠狀物質,既能與強酸反應,也能與強堿反應,具有凈水作用.各物質間的轉化關系如圖所示(某些條件巳略去).
已知 A、B、D為中學常見的單質,甲、乙、丙、丁、戊為短周期元素組成的化合物.其中,丙是一種能使濕潤的紅色石蕊試紙變藍的無色氣體;丁是一種高能燃料,其組成元素與丙相同,1mol 丁分子中不同原子的數目比為1:2,且含有18mol電子;戊是一種難溶于水的白色膠狀物質,既能與強酸反應,也能與強堿反應,具有凈水作用.各物質間的轉化關系如圖所示(某些條件巳略去).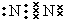 .寫出丙的結構式
.寫出丙的結構式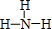 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol Cl2參加反應,轉移的電子數一定為2NA | |
| B. | 常溫常壓下,23g NO2與N2O4的混合氣體中氮原子數為0.5NA | |
| C. | 標準狀況下,22.4L乙烯中含極性共價鍵數為4NA | |
| D. | 2L 0.1mol•L-1的HClO溶液中含有的H+離子數小于0.2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 取溶液進行焰色反應顯黃色,一定含有Na+ | |
| B. | 滴加BaCl2溶液,產生白色沉淀,證明有SO42- | |
| C. | 滴加KSCN溶液,變為血紅色,溶液中含Fe2+ | |
| D. | 加入稀鹽酸產生無色氣體,一定含有CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、K+、Cl-、F- | B. | Fe2+、ClO-、NO3-、Na+ | ||
| C. | Fe2+、Mg2+、SO42-、Cl- | D. | CO32-、SO42-、Na+、K+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有②③ | B. | ①②③ | C. | ②③④ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
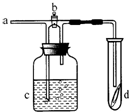 如圖所示,從a處通入了氯氣.若打開活塞b,d處的干燥有色布條不褪色,若關閉活塞b,d處的干燥有色布條褪色.下列判斷正確的是( )
如圖所示,從a處通入了氯氣.若打開活塞b,d處的干燥有色布條不褪色,若關閉活塞b,d處的干燥有色布條褪色.下列判斷正確的是( )| A. | c中盛放的不可能是NaCl溶液 | B. | c中盛放的可能是濃硫酸 | ||
| C. | c中盛放的可能是足量NaOH溶液 | D. | a處通入的是干燥的氯氣 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com