
分析 (1)摩爾質量以g/mol為單位,數值上等于其相對分子質量;根據n=$\frac{m}{M}$計算水的物質的量;根據V=nVm計算氧氣體積;根據n=$\frac{m}{M}$計算NaOH的物質的量,再根據c=$\frac{n}{V}$計算溶液物質的量濃度;
(2)根據氯離子物質的量計算RCl2的物質的量,再根據M=$\frac{m}{n}$計算其摩爾質量,進而計算A的相對原子質量.
解答 解:(1)二氧化碳的相對分子質量為44,則二氧化碳摩爾質量為44 g•mol-1;
水的摩爾質量為18g/mol,9g水的物質的量是$\frac{9g}{18g/mol}$=0.5mol;
0.5molO2在標準狀況下的體積約為0.5mol×22.4L/mol=11.2L;約含有0.5mol×2×NA=NA,20g燒堿的物質的量為$\frac{20g}{40g/mol}$=0.5mol,配制成500mL溶液,其物質的量濃度為$\frac{0.5mol}{0.5L}$=1mol/L.
故答案為:44 g•mol-1; 0.5mol;11.2L;NA;1;
(2)19g某二價金屬氯化物(RCl2)中含有0.4mol Cl-,則RCl2的物質的量為$\frac{0.4mol}{2}$=0.2mol,RCl2的摩爾質量是$\frac{19g}{0.2mol}$=95 g•mol-1,相對分子質量是為95,則R的相對原子質量為95-35.5×2=24,
故答案為:95 g•mol-1;24.
點評 本題考查物質的量有關計算,比較基礎,注意掌握以物質的量為中心有關計算,有利于基礎知識的鞏固.


 全優考典單元檢測卷及歸類總復習系列答案
全優考典單元檢測卷及歸類總復習系列答案 品學雙優卷系列答案
品學雙優卷系列答案 小學期末沖刺100分系列答案
小學期末沖刺100分系列答案科目:高中化學 來源: 題型:選擇題
| A. | 從左向右數第六縱行是ⅥA族 | B. | 七個周期18個族 | ||
| C. | ⅠA族全部是金屬元素 | D. | 所含元素種類最多的族是ⅢB族 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  實驗測定氯水的pH | |
| B. | 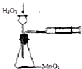 實驗定量測定H2O2的分解速率 | |
| C. | 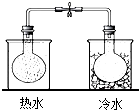 實驗中利用NO2顏色的變化驗證其中反應的熱效應 | |
| D. | 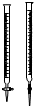 實驗中(乙)管內盛放已知濃度的KMnO4溶液來測定FeSO4溶液的濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2CO3 | B. | NaHCO3 | C. | Na2CO3 和NaHCO3 | D. | NaOH和Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 150ml 1mol/L的NaCl溶液 | B. | 150ml 3mol/LKCl溶液 | ||
| C. | 75ml 2mol/L的NH4Cl溶液 | D. | 50ml 1mol/lCuCl2溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 I2在KI溶液中存在平衡:I2(aq)+I-(aq)═I3- (aq),某I2、KI混合溶液中,c(I3-)與溫度T的平衡曲線圖如下.下列說法不正確的是( )
I2在KI溶液中存在平衡:I2(aq)+I-(aq)═I3- (aq),某I2、KI混合溶液中,c(I3-)與溫度T的平衡曲線圖如下.下列說法不正確的是( )| A. | 反應I2(aq)+I-(aq)═I3- (aq)的△H>0 | |
| B. | 若溫度為T1、T2,反應的平衡常數分別為K1、K2,則K1>K2 | |
| C. | 若反應進行到狀態D時,一定有v正>v逆 | |
| D. | 狀態A與狀態B相比,狀態A的c(I2) 小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
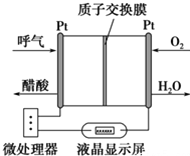 如圖所示是一種酸性燃料電池酒精檢測儀,具有自動吹氣流量偵測與控制的功能,非常適合進行現場酒精檢測.下列說法不正確的是( )
如圖所示是一種酸性燃料電池酒精檢測儀,具有自動吹氣流量偵測與控制的功能,非常適合進行現場酒精檢測.下列說法不正確的是( )| A. | 該電池的負極反應式為:CH3CH2OH+3H2O-12e-═2CO2↑+12H+ | |
| B. | 該電池的正極反應式為:O2+4e-+4H+═2H2O | |
| C. | 電流由O2所在的鉑電極經外電路流向另一電極 | |
| D. | 微處理器通過檢測電流大小而計算出被測氣體中酒精的含量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子序數:D>C>B>A | B. | 氫化物的穩定性:H2C>HD | ||
| C. | 離子半徑:C2->D->B+>A2+ | D. | 氧化性:A2+>B+,還原性:C2-<D- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始濃度(mol•L-1) | 2.0 | 1.0 | 0 |
| 平衡濃度(mol•L-1) | c1 | c2 | 0.4 |
| A. | 10 min內,v(Cl2)=0.04 mol•L-1•min-1 | |
| B. | 當容器中Cl2為1.2 mol時,反應達到平衡 | |
| C. | 升高溫度(T1<T2),反應的平衡常數減小,平衡時PCl3$\frac{△n({T}_{1})}{△n({T}_{2})}$<1 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同條件再達平衡時,c(PCl5)<0.2 mol•L-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com