
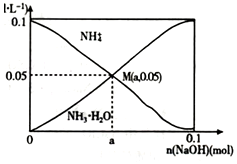
 常溫下,向1L0.lmol•L-1NH4Cl溶液中,不斷加入固體NaOH后,NH4+與NH3•H20的變化趨勢如圖 所示(不考慮溶液體積的變化和氨的揮發),下列說法正確的是( )
常溫下,向1L0.lmol•L-1NH4Cl溶液中,不斷加入固體NaOH后,NH4+與NH3•H20的變化趨勢如圖 所示(不考慮溶液體積的變化和氨的揮發),下列說法正確的是( )| A. | M點溶液中水的電離程度比原溶液大 | |
| B. | 在 M 點時,n(OH- )-n(H+)=(a-0.05)mol | |
| C. | 當n(NaOH)=0.05mol時溶液中有:c(Cl-)>c(Na+)>c( NH4+)>c(OH-)>c(H+) | |
| D. | 隨著NaOH的加入,一定存在c(Cl-)+c(0H-)+c(NH3•H20)>0.lmol•L-1 |
分析 A.M點是向1L 0.1mol•L-1NH4Cl溶液中,不斷加入NaOH固體后反應得到氯化銨和一水合氨溶液,銨根離子濃度和一水合氨濃度相同,一水合氨是一元弱堿抑制水電離;
B.依據溶液中電荷守恒分析判斷,n(Na+)=amol,n(Cl-)=1mol;
C.向1L 0.1mol•L-1NH4Cl溶液中,不斷加入NaOH固體后,當n(NaOH)=0.05mol時,得到物質的量均為0.05molNH4Cl、0.05molNaCl和0.05molNH3•H2O的混合物;
D.原溶液中存在物料守恒,c(NH4+)+c(NH3•H20)=0.1mol/L.
解答 解:A.M點是向1L 0.1mol•L-1NH4Cl溶液中,不斷加入NaOH固體后反應得到氯化銨和一水合氨溶液,銨根離子濃度和一水合氨濃度相同,一水合氨是一元弱堿抑制水電離,此時水的電離程度小于原氯化銨溶液中水的電離程度,故A錯誤;
B.在M點時溶液中存在電荷守恒,n(0H-)+n(Cl-)=n(H+)+n(Na+)+n(NH4+),n(0H-)-n(H+)=0.05+n(Na+)-n(Cl-)=(a-0.05)mol,故B正確;
C.向1L 0.1mol•L-1NH4Cl溶液中,不斷加入NaOH固體后,當n(NaOH)=0.05mol時,得到物質的量均為0.05molNH4Cl、0.05molNaCl和0.05molNH3•H2O的混合物,由于NH3•H2O電離大于NH4Cl水解,故離子濃度大小關系為:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),故D錯誤;
D.1L0.lmol•L-1NH4Cl溶液中,存在物料守恒c(NH4+)+c(NH3•H20)=0.1mol/L,隨著NaOH的加入,一定存在c(Cl-)+c(0H-)+c(NH3•H20)>0.lmol•L-1,故D正確;
故選BD.
點評 本題考查了酸堿反應過程分析,主要是溶液酸堿性、離子濃度大小,對水的電離影響因素分析判斷,題目難度中等.


科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含有大量ClO-的溶液中:K+、OH-、I-、SO32- | |
| B. | pH值為1的溶液:Cu2+、Na+、Mg2+、NO3- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的溶液中:NH4+、Al3+、NO3-、CO32- | |
| D. | 由水電離的c(H+)=1.0×10-13 mol•L-1的溶液中:K+、NH4+、AlO2-、HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 美國阿波羅宇宙飛船上使用的氫氧燃料電池是一種新型化學電源,其構造如圖所示:a、b兩個極均由多孔性碳制成,通入的氣體由孔隙中逸出,并在電極表面放電.
美國阿波羅宇宙飛船上使用的氫氧燃料電池是一種新型化學電源,其構造如圖所示:a、b兩個極均由多孔性碳制成,通入的氣體由孔隙中逸出,并在電極表面放電.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=2的溶液中:S2O32-、K+、Cl-、Na+ | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=10-10 mol/L的溶液中:Na+、HCO3-、Cl-、K+ | |
| C. | 在$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3- | |
| D. | 由水電離產生的c(OH-)=1×10-12mol/L的溶液中:NO3-、Mg2+、Na+、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 反應類型 | 反應條件 |
| A | 加成、取代、消去 | KOH醇溶液/加熱、KOH水溶液/加熱、常溫 |
| B | 消去、加成、取代 | NaOH醇溶液/加熱、常溫、KOH水溶液/加熱 |
| C | 氧化、取代、消去 | 加熱、KOH醇溶液/加熱、KOH水溶液/加熱 |
| D | 消去、加成、水解 | NaOH水溶液/加熱、常溫、NaOH醇溶液/加熱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④ | B. | ③④⑤ | C. | ①②④⑤ | D. | ①②③④ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com