
 TiO2•xH2O↓+4HCl△H>0可知,加入大量水并加熱,都能使水解反應向正反應方向進行,促進水解趨于完全;
TiO2•xH2O↓+4HCl△H>0可知,加入大量水并加熱,都能使水解反應向正反應方向進行,促進水解趨于完全;| TiCl4 | Mg | MgCl2 | Ti | |
| 熔點/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸點/℃ | 136.4 | 1090 | 1412 | 3287 |
分析 (1)Ti的原子序數為22,比Ca的原子序數多2,以此判斷;
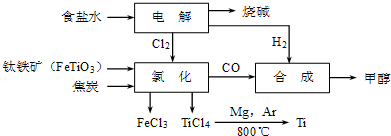
(2)鈦鐵礦在高溫下與焦炭、氯氣反應得到四氯化鈦,同時生成氯化鐵和CO;
(3)TiCl4水解生成TiO2•xH2O,再經焙燒制得TiO2,水解為吸熱反應,從平衡移動角度分析;
(4)在Ar氣中進行防止鈦、鎂被氧化;控制溫度使TiCl4、Mg、MgCl2轉化為蒸氣,Ti不融化;
(5)根據甲醇的物質的量計算需要CO、H2的物質的量,根據n(CO)計算電解中生成的n(Cl2),進而計算電解生成n(H2),據此計算解答.
解答 解:(1)Ti的原子序數為22,比Ca的原子序數多2,應位于周期表第四周期族ⅣB,故答案為:四;ⅣB;
(2)鈦鐵礦在高溫下與焦炭、氯氣反應得到四氯化鈦,同時生成氯化鐵和CO,反應的化學方程式為2FeTiO3+6C+7Cl2$\frac{\underline{\;高溫\;}}{\;}$2FeCl3+2TiCl4+6CO,
故答案為:2FeTiO3+6C+7Cl2$\frac{\underline{\;高溫\;}}{\;}$2FeCl3+2TiCl4+6CO;
(3)水解時需加入大量的水并加熱,由TiCl4+(2+x) H2O TiO2•xH2O↓+4HCl△H>0可知,加入大量水并加熱,都能使水解反應向正反應方向進行,促進水解趨于完全,
TiO2•xH2O↓+4HCl△H>0可知,加入大量水并加熱,都能使水解反應向正反應方向進行,促進水解趨于完全,
故答案為:由TiCl4+(2+x) H2O TiO2•xH2O↓+4HCl△H>0可知,加入大量水并加熱,都能使水解反應向正反應方向進行,促進水解趨于完全;
TiO2•xH2O↓+4HCl△H>0可知,加入大量水并加熱,都能使水解反應向正反應方向進行,促進水解趨于完全;
(4)在Ar氣中進行防止鈦、鎂被氧化;控制溫度使TiCl4、Mg、MgCl2轉化為蒸氣,Ti不熔化,故溫度略高于1412℃蒸餾可分離,
故答案為:防止鈦、鎂被氧化;蒸餾;1412;
(5)由CO和H2合成甲醇的方程式是CO(g)+2H2(g)?CH3OH(g),合成6mol甲醇需要n(CO)=6mol、n(H2)=12mol.根據2FeTiO3+6C+7Cl2$\frac{\underline{\;高溫\;}}{\;}$2FeCl3+2TiCl4+6CO可知,電解中生成的n(Cl2)=$\frac{7}{6}$n(CO)=7mol,根據2NaCl+2H2O$\frac{\underline{\;通電\;}}{\;}$2NaOH+H2↑+Cl2↑可知,電解生成n(H2)=n(Cl2)=7mol,故需額外補充H2 為12mol-7mol=5mol,
故答案為:CO(g)+2H2(g)?CH3OH(g);5.
點評 本題的綜合性很強,側重分析能力及計算能力的考查,涉及化學反應方程式的書寫,燃燒熱等多方面內容,注意知識的遷移應用,對學生能力要求較高,題目難度較大.


科目:高中化學 來源: 題型:解答題
 常溫下有下列四種溶液:
常溫下有下列四種溶液:| 序號 | ① | ② | ③ | ④ |
| 溶液 | pH=4的NH4Cl溶液 | pH=4的鹽酸 | 0.1mol•L-1的醋酸溶液 | 0.1mol•L-1的NaOH溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向Na2S溶液中加入少量的氯化銀:S2-+2Ag+═Ag2S↓ | |
| B. | 向滴有酚酞的1 mol/L硅酸鈉溶液中加入稀鹽酸至溶液紅色消失:SiO${\;}_{3}^{2-}$+2H+═H2SiO3(膠體) | |
| C. | 碳酸氫銨溶液中加入足量NaOH:HCO${\;}_{3}^{-}$+OH-═CO${\;}_{3}^{2-}$+H2O | |
| D. | 向苯酚鈉溶液中通入一定量CO2: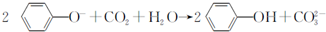 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
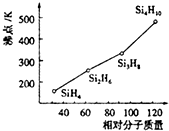 太陽能電池是通過光電效應或者光化學效應直接把光能轉化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.
太陽能電池是通過光電效應或者光化學效應直接把光能轉化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
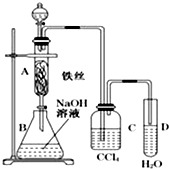 某化學課外小組用圖所示裝置制取溴苯.先向分液漏斗中加入苯和液溴,再將混合液慢慢滴入反應器A(A下端活塞關閉)中.
某化學課外小組用圖所示裝置制取溴苯.先向分液漏斗中加入苯和液溴,再將混合液慢慢滴入反應器A(A下端活塞關閉)中.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaCl晶體、BaSO4 | B. | 鋁、二氧化硫 | ||
| C. | 液態的醋酸、酒精 | D. | 熔融的KNO3、硫酸溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | △H>0的反應一定不能自發進行 | |
| B. | 同溫、同濃度的鹽酸和氫氧化鈉稀溶液中,水的電離程度相同 | |
| C. | 為保護浸入海水中的鋼閘門,可在閘門表面鑲上銅錠 | |
| D. | 硫酸工業中二氧化硫的催化氧化生成三氧化硫,不采用高壓是因為壓強對SO2轉化率無影響 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | H2 | CO | CH4 |
| 燃燒熱(kJ•mol-1) | 285.8 | 283.0 | 890.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗 | 實驗現象 | 結論 |
| A | 無色溶液變藍 | I-在酸性條件下被氧氣氧化為I2 |
| B | 溶液均呈紅色,且深淺一樣 | 相同濃度的CO32-與HCO3-水解能力相同 |
| C | 產生白色沉淀又逐漸變成紅褐色沉淀 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 溴的四氯化碳溶液顏色褪去 | 石蠟催化加熱反應產物為乙烯 |
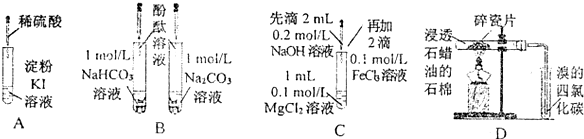
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com