
| A. | NaHSO4溶液與Ba(OH)2溶液反應 | B. | C6H5ONa溶液與CO2反應 | ||
| C. | NaAlO2溶液與CO2反應 | D. | Fe與稀硝酸反應 |
分析 A.硫酸氫鈉過量與不足時,反應的離子方程式不同;
B.苯酚的酸性大于碳酸氫根離子,則苯酚鈉與二氧化碳反應生成苯酚和碳酸氫鈉;
C.二氧化碳過量時,反應生成碳酸氫鈉和氫氧化鋁沉淀,二氧化碳步驟時生成碳酸鈉;
D.鐵與稀硝酸反應,當鐵過量或不足時,反應產物不同.
解答 解:A.NaHSO4溶液與Ba(OH)2溶液反應,當硫酸氫鈉不足時,離子方程式按照硫酸氫鈉的化學式書寫,其反應的離子方程式為:H++SO42-+Ba2++OH-=BaSO4↓+H2O;當硫酸氫鈉過量時,離子方程式按照氫氧化鋇的化學式組成書寫,反應的離子方程式為:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,改變反應物的量后離子方程式不同,故A錯誤;
B.由于苯酚的酸性大于碳酸氫根離子,則苯酚鈉與二氧化碳反應生成碳酸氫鈉和苯酚,反應的離子方程式為:C6H5O-+CO2+H2O→C6H5OH+HCO3-,與反應物的量無關,故B正確;
C.當二氧化碳不足時,反應生成氫氧化鋁沉淀和碳酸鈉,反應的離子方程式為:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,當二氧化碳過量時,反應生成氫氧化鋁沉淀和碳酸氫鈉,反應為:AlO2-+CO2+2H2O→Al(OH)3↓+HCO3-,反應產物與二氧化碳的過量情況有關,故C錯誤;
D.過量的鐵與稀硝酸反應生成硝酸亞鐵:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O,若鐵不足時生成硝酸鐵:Fe+4H++NO3-═Fe3++NO↑+2H2O,鐵的過量情況影響反應產物及離子方程式,故D錯誤;
故選B.
點評 本題考查了離子方程式書寫判斷,題目難度中等,明確離子方程式的書寫原則及發生反應實質為解答關鍵,注意掌握反應物過量情況對生成產物的影響,試題培養了學生靈活應用基礎知識的能力.


科目:高中化學 來源: 題型:解答題

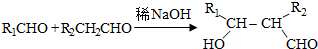
 .
. .
.
 (寫結構簡式)
(寫結構簡式)查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 液晶態介于晶體狀態和液態之間,液晶具有一定程度的晶體的有序性和液體的流動性 | |
| B. | 常壓下,0℃時冰的密度比水的密度小,水在4℃時密度最大,這些都與分子間的氫鍵有關 | |
| C. | 石油裂解、煤的干餾、玉米制醇、蛋白質的變性和納米銀粒子的聚集都是化學變化 | |
| D. | 燃料的脫硫脫氮、SO2的回收利用和NOx的催化轉化都是減少酸雨產生的措施 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| Ca2+ | Mg2+ | Fe3+ | |
| 開始沉淀時的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀時的pH | 13.9 | 11.1 | 3.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
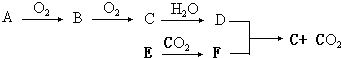
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2S溶液中,2c(Na+)=c(S2-)+c(HS-)+c(H2S) | |
| B. | 強堿弱酸鹽NaA溶液的pH=8,則c(OH-)-c(HA)=1,0×10-8mol/L | |
| C. | KAl(SO4)2溶液中,c(SO42-)>c(K+)=c(Al3+)>c(H+)>c(OH-) | |
| D. | 向100ml pH=12 的 NaOH溶液中加入pH=2的醋酸溶液至中性,所得溶液的總體積大于200ml |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.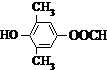 或
或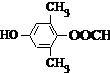 .
.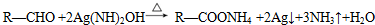 .
.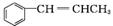 為原料制備
為原料制備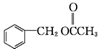 的合成路線流程圖如下,試在方框內補充有機物的結構簡式:
的合成路線流程圖如下,試在方框內補充有機物的結構簡式:
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

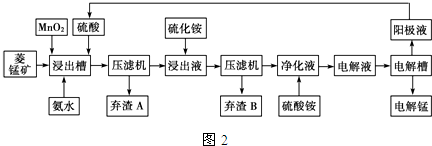
| 物質 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 | Fe(OH)3 |
| 開始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 | 2.7 |
| 完全沉淀pH | 9.7 | 8.4 | 8.2 | 9.8 | 3.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
 短周期元素X、Y、Z、W在周期表中的相對位置如圖,W原子的最外層電子數是其最內層電子數的3倍.下列判斷正確的是( )
短周期元素X、Y、Z、W在周期表中的相對位置如圖,W原子的最外層電子數是其最內層電子數的3倍.下列判斷正確的是( )| A. | 原子半徑:Y>Z>X | |
| B. | 含Y元素的鹽溶液有的顯酸性,有的顯堿性 | |
| C. | 最簡單氣態氫化物的熱穩定性:Z>W | |
| D. | X與R的核電荷數相差24 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com