
| A、Na+ K+ HCO3- Cl- |
| B、NH4+ Mg2+ SO42- Cl- |
| C、K+ Na+ SO42- CH3COO- |
| D、K+ Ca2+ CO32- NO3- |


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
| A、Br->Fe2+>I- |
| B、I->Fe2+>Br- |
| C、Br->I->Fe2+ |
| D、Fe2+>I->Br- |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 實驗步驟 | 實驗操作 |
| Ⅰ | 取一定質量的FeCO3固體置于坩堝中,高溫煅燒至質量不再減輕,冷卻至室溫. |
| Ⅱ | 取少量實驗步驟Ⅰ所得固體放于一潔凈的試管中,用足量的稀硫酸溶解. |
| Ⅲ | 向實驗步驟Ⅱ所得溶液中滴加KSCN溶液,溶液變紅. |
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
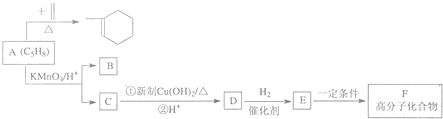
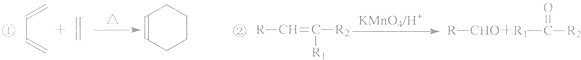
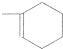 時,A發生的反應類型為
時,A發生的反應類型為查看答案和解析>>
科目:高中化學 來源: 題型:
A、氟離子的結構示意圖: |
B、CH4的比例模型: |
C、羧基的電子式: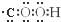 |
| D、NaHCO3的電離方程式:NaHCO3═Na++H++CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:
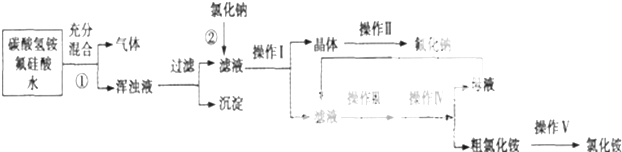
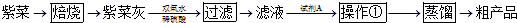
| 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶體) | |
| 密度/g、cm-3 | 0.7893 | 1.595 | 0.71~0.76 | 4.94 |
| 沸點/℃ | 78.5 | 76.8 | 25~232 | 184.35 |
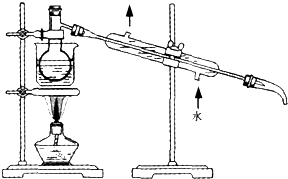
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、接觸法制硫酸:氧化爐、硫鐵礦、V2O5、400℃-500℃ |
| B、聯合制堿法制純堿:吸氨塔、碳酸塔、食鹽、二氧化碳、氨、30℃-35℃的氨化飽和食鹽水吸收二氧化碳 |
| C、合成氨:沸騰爐、焦炭、鐵觸媒、500℃ |
| D、氨氧化法制硝酸:合成塔、空氣、鉑銠合金、800℃ |
查看答案和解析>>
科目:高中化學 來源: 題型:
 隨著能源與環境問題越來越被人們關注,碳一化學(C1化學)成為研究的熱點.“碳一化學”即以單質碳及CO、CO2、CH4、CH3OH等含一個碳原子的物質為原料合成工業產品的化學與工藝.
隨著能源與環境問題越來越被人們關注,碳一化學(C1化學)成為研究的熱點.“碳一化學”即以單質碳及CO、CO2、CH4、CH3OH等含一個碳原子的物質為原料合成工業產品的化學與工藝.
| ||
| 催化劑 |
| △ |
| 催化劑 |
| △ |
| 催化劑 |
| △ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com