
| 操 作 | 現 象 |
| 取4g漂粉精固體,加入100mL水 | 部分固體溶解,溶液略有顏色 |
| 過濾,測漂粉精溶液的pH | pH試紙先變藍(約為12),后褪色 |
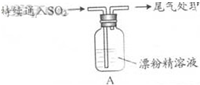 | i.液面上方出現白霧; ii.稍后,出現渾濁,溶液變為黃綠色; iii.稍后,產生大量白色沉淀,黃綠色褪去 |
分析 (1)氯氣和氫氧化鈣反應生成氯化鈣、次氯酸鈣和水;
(2)pH試紙變藍色,說明溶液呈堿性,次氯酸具有漂白性;
(3)①氯氣能使濕潤的淀粉碘化鉀試紙變藍色;
②SO2可以使酸化的AgNO3溶液產生白色沉淀;
(4)根據其它酸是否溶液變為黃綠色;
(5)①SO2被氧化為SO42-,硫酸根離子和鈣離子結合生成微溶物硫酸鈣;
②溶液呈黃綠色,有Cl2生成,Cl2與SO2反應生成鹽酸與硫酸,據此書寫.
解答 解:(1)Cl2和Ca(OH)2生成氯化鈣、次氯酸鈣與水,反應方程式為2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案為:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(2)pH試紙先變藍(約為12),說明溶液呈堿性,后顏色褪去,說明又具有漂白性,故答案為:堿性、漂白性;
(3)①反應中生成Cl2,用濕潤的碘化鉀淀粉試紙檢驗白霧中是否含有Cl2,排除Cl2干擾,故答案為:檢驗白霧中是否含有Cl2,排除Cl2干擾;
②白霧中含有SO2,可以被硝酸氧化為硫酸,硫酸與AgNO3溶液反應產生硫酸銀白色沉淀,故SO2可以使酸化的AgNO3溶液產生白色沉淀,
故答案為:白霧中含有SO2,SO2可以使酸化的AgNO3溶液產生白色沉淀;
(4)向漂白精溶液中逐滴滴入硫酸,觀察溶液顏色是否變為黃綠色,故答案為:向漂粉精溶液中逐滴滴入硫酸,觀察溶液顏色是否變為黃綠色;
(5)①取上層清液,加入BaC12溶液,產生白色沉淀,說明SO2被氧化為SO42-,故沉淀X為CaSO4,故答案為:CaSO4;
②溶液呈黃綠色,有Cl2生成,Cl2與SO2反應生成鹽酸與硫酸,反應方程式為Cl2+SO2+2H2O=4H++2Cl-+SO42-,故答案為:Cl2+SO2+2H2O=4H++2Cl-+SO42-.
點評 本題考查探究實驗,根據實驗現象分析物質的性質,同時考查學生分析問題、總結問題能力,注意:不能用pH試紙測定氯水pH值,次氯酸有漂白性導致測定不準確,為易錯點.


科目:高中化學 來源: 題型:選擇題
| A. | $\frac{3n+2}{2}$ | B. | $\frac{3n-2}{2}$ | C. | $\frac{2n-2}{3}$ | D. | n+1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe3+、Mg2+、SO42-、Cl- | B. | Ba2+、K+、I-、NO3- | ||
| C. | Fe2+、Cu2+、AlO2-、ClO- | D. | Na+、Ca2+、Cl-、CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 如圖是一個實驗室制取氯氣并以氯氣為原料進行特定反應的裝置.
如圖是一個實驗室制取氯氣并以氯氣為原料進行特定反應的裝置.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
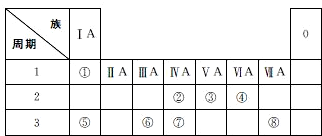
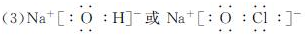 .
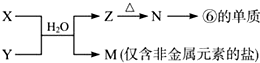
.
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
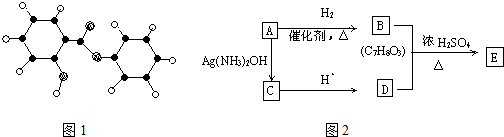

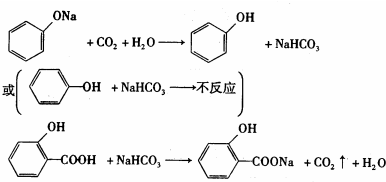 .
.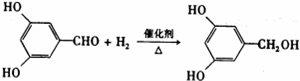 ;反應類型:加成反應.
;反應類型:加成反應.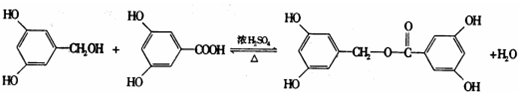 ;反應類型:酯化反應
;反應類型:酯化反應查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 室溫下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42- | |
| B. | 含有0.1mol•L-1Fe3+的溶液中:K+、Mg2+、I-、NO3- | |
| C. | 無色溶液中:K+、Na+、MnO4-、SO42- | |
| D. | pH=11的溶液中:CO32-、Na+、AlO2-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用濕潤的pH試紙測稀堿液的,測定值偏小 | |
| B. | 用量筒量取10mLNaOH 溶液時,俯視刻度.量出的體積大于10mL | |
| C. | 使用天平稱量時不小心將藥品與砝碼的位置放反了,稱最結果可能是準確的 | |
| D. | 測定中和反應的反應熱時,將堿緩慢倒入酸中,所測溫度值偏小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com