
【題目】金屬及其化合物的種類很多,我們可以按照“金屬單質、金屬氧化物、金屬氫氧化物、鹽”的類別進行研究。以下是元素周期表中前18號某種金屬元素對應的單質及其化合物之間的轉化關系(“→”所指的轉化都是一步完成)。
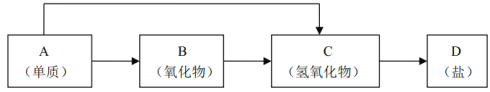
(1)A與水反應的離子方程式:_______________。
(2)若B為呼吸面具中的供氧劑,其供氧時每生成1molO2,反應過程中轉移的電子數為____________。
(3)200℃時,11.6gCO2和H2O的混合物氣體與足量的B反應,反應后固體增加了3.6g,則原混合物的平均相對分子質量為__________。
(4)寫出一種“C→D”轉化的離子方程式:____。
(5)某同學將一小塊A單質露置于空氣中,觀察到下列現象:銀白色![]() 變灰暗
變灰暗![]() 變白色
變白色![]() 出現液滴
出現液滴![]() 白色固體,則下列說法正確的是_________。
白色固體,則下列說法正確的是_________。
A.①發生了氧化還原反應
B.①變灰暗色是因為生成了過氧化鈉
C.③是碳酸鈉吸收空氣中的水蒸氣形成了溶液
D.④只發生物理變化
【答案】2Na+2H2O=2Na++2OH-+H2↑ 2NA或2×6.02×1023 23.2 OH-+H+=H2O(答案合理即可) A
【解析】
金屬單質可以形成氧化物,也可以直接生成氫氧化物、金屬氧化物可以生成氫氧化物、金屬氫氧化物一步形成鹽,根據金屬單質可以直接形成堿,說明A為活潑金屬Na、Mg等,但氧化鎂不能溶于水生成氫氧化鎂,因此A為Na元素。結合鈉及其化合物的性質分析解答。
根據框圖,金屬單質A能夠一步反應生成C(氫氧化物),則A為活潑金屬Na、Mg等,但氧化鎂不能溶于水生成氫氧化鎂,因此A為Na,C為NaOH。
(1)A為鈉,Na與水反應的化學方程式為:2Na+2H2O=2NaOH+H2↑,離子方程式為:2Na+2H2O=2Na++2OH-+H2↑,故答案為:2Na+2H2O=2Na++2OH-+H2↑;
(2)若B為呼吸面具中的供氧劑,則B為Na2O2,其供氧時主要反應的化學方程式為2Na2O2+2CO2=2Na2CO3+O2和2Na2O2 + 2H2O = 4NaOH + O2↑,兩個反應中都是只有過氧化鈉中的O元素化合價發生變化,其供氧時每生成1mol O2,反應過程中轉移的電子數為2NA或2×6.02×1023,故答案為:2NA或2×6.02×1023;
(3)由反應:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,可知參加反應的CO2和H2O與生成O2的物質的量之比為2∶1,m(增重)=m(吸收)-m(放出),即11.6g-m(O2)=3.6g,m(O2)=11.6g-3.6g=8.0g,所以n(O2)=![]() =0.25mol,n(CO2和H2O)=0.5mol,則原混合氣體的平均摩爾質量為
=0.25mol,n(CO2和H2O)=0.5mol,則原混合氣體的平均摩爾質量為![]() =23.2g/mol,原混合物的平均相對分子質量為23.2,故答案為:23.2;
=23.2g/mol,原混合物的平均相對分子質量為23.2,故答案為:23.2;
(4)如C→D轉化的化學方程式為:NaOH+HCl=NaCl+H2O,則離子方程式為:OH-+H+=H2O,故答案為:OH-+H+=H2O;
(5)Na的性質活潑,易與空氣中氧氣反應生成Na2O,Na2O易與水反應生成NaOH,NaOH吸收空氣中的水和CO2生成Na2CO3xH2O,Na2CO3xH2O風化脫水生成Na2CO3。A.①發生氧化還原反應生成了氧化鈉,故A正確;B.①變灰暗色主要是因為生成了氧化鈉,4Na+O2=2Na2O,故B錯誤;C.③是氫氧化鈉潮解,吸收水蒸氣形成氫氧化鈉溶液,故C錯誤;D.④是二氧化碳和氫氧化鈉反應生成碳酸鈉固體,發生了化學反應,故D錯誤;故答案為:A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】現有19.2克銅與400毫升稀硝酸發生如下反應3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)用雙線橋表示出電子轉移的方向和數目_____________
(2)計算稀硝酸的物質的量濃度_____________
(3)計算產生的氣體在標況下的體積_____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬(M)–空氣電池(如圖)具有原料易得、能量密度高等優點,有望成為新能源汽車和移動設備的電源。該類電池放電的總反應方程式為:4M+nO2+2nH2O=4M(OH) n。已知:電池的“理論比能量”指單位質量的電極材料理論上能釋放出的最大電能。下列說法不正確的是

A. 采用多孔電極的目的是提高電極與電解質溶液的接觸面積,并有利于氧氣擴散至電極表面
B. 比較Mg、Al、Zn三種金屬–空氣電池,Al–空氣電池的理論比能量最高
C. M–空氣電池放電過程的正極反應式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
D. 在M–空氣電池中,為防止負極區沉積Mg(OH)2,宜采用中性電解質及陽離子交換膜
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(2017·天津卷)常壓下羰基化法精煉鎳的原理為:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃時,該反應的平衡常數K=2×105。已知:Ni(CO)4的沸點為42.2℃,固體雜質不參與反應。
Ni(CO)4(g)。230℃時,該反應的平衡常數K=2×105。已知:Ni(CO)4的沸點為42.2℃,固體雜質不參與反應。
第一階段:將粗鎳與CO反應轉化成氣態Ni(CO)4;
第二階段:將第一階段反應后的氣體分離出來,加熱至230℃制得高純鎳。
下列判斷正確的是
A. 增加c(CO),平衡向正向移動,反應的平衡常數增大
B. 第二階段,Ni(CO)4分解率較低
C. 第一階段,在30℃和50℃兩者之間選擇反應溫度,選50℃
D. 該反應達到平衡時,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是( )
A. 1 mol Cl2參加反應轉移電子數一定為2NA
B. 在反應KIO3+6HI=KI+3I2+3H2O中,每生成3 mol I2轉移的電子數為6NA
C. 根據反應中HNO3(稀)![]() NO,而HNO3(濃)
NO,而HNO3(濃)![]() NO2可知,氧化性:HNO3(稀)>HNO3(濃)
NO2可知,氧化性:HNO3(稀)>HNO3(濃)
D. 含有大量NO3—的溶液中,不能同時大量存在H+、Fe2+、Cl-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銀鋅紐扣電池如圖,電池反應式為:![]() ,下列說法正確的是( )
,下列說法正確的是( )
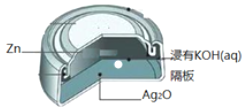
A.鋅作負極
B.電池工作時,電流從Zn經導線流向Ag2O
C.正極發生還原反應
D.負極的電極反應式為:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】寫出下列有機物的系統命名或結構簡式:
(1) ![]() _________________
_________________
(2)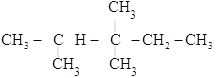 ________________
________________
(3)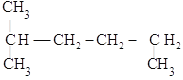 __________
__________
(4)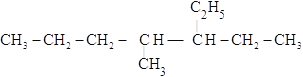 ______________
______________
(5)2,2-二甲基-3-乙基己烷____________________
(6)1,1,2,2-四氯丙烷____________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組為測定放置已久的小蘇打樣品中純堿的質量分數,設計如下實驗方案:
(1)方案一:稱取一定質量的樣品,置于坩堝中加熱至恒重后,冷卻,稱取剩余固體質量,計算。
①完成本實驗需要不斷用玻璃棒攪拌,其目的是_______________________________。
②若實驗前所稱樣品的質量為m g,加熱至恒重時固體質量為a g,則樣品中純堿的質量分數為________。
(2)方案二:按如圖所示裝置進行實驗,并回答下列問題:
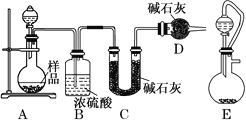
①實驗前先檢查裝置的氣密性,并稱取一定質量的樣品放入A中,將稀硫酸裝入分液漏斗中。D裝置的作用是________________。
②實驗中除稱量樣品質量外,還需分別稱量_______裝置反應前、后質量(填裝置字母代號)。
③根據此實驗得到的數據,測定結果有誤差。因為實驗裝置還存在一個明顯的缺陷,該缺陷是_________。
④有同學認為,用E裝置替代A裝置能提高實驗準確度。你認為是否正確?_________(填“是”或“否”)。
(3)方案三:稱取一定量的樣品置于錐形瓶中,加適量水,用鹽酸進行滴定,從開始至有氣體產生到氣體不再產生,所滴加的鹽酸體積如圖所示,則小蘇打樣品中純堿的質量分數為_________(保留兩位有效數字)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】主族元素碳、氧、氮、氟、磷、硒及副族元素鎳、銅元素在化學中有很重要的地位,回答下列問題:
(1)在基態14C原子中,核外存在___對自旋相反的電子,基態氮原子的價層電子排布圖為____。
(2)將F2通入稀NaOH溶液中可生成OF2,OF2分子構型為__其中氧原子的雜化方式為_______。
(3)CuSO4溶液能用作P4中毒的解毒劑,反應可生成P的最高價含氧酸和銅,該反應的化學方程式是_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com