
(10分)氫化鈣(CaH2,其中H元素的化合價為 –1價)固體是登山運動員常用的能源提供劑。氫化鈣要密封保存,一旦接觸到水就發生反應生成氫氧化鈣和氫氣。氫化鈣通常用氫氣與金屬鈣加熱制取,下圖是模擬制取裝置。
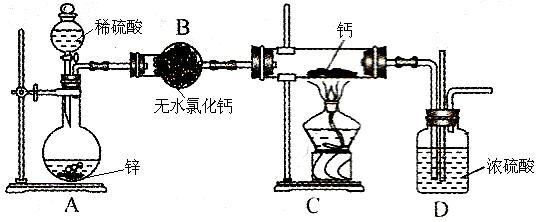
(1)氫化鈣與水反應的化學方程式為:__________________。
該反應中氧化產物與還原產物的物質的量之比為:__________________。
(2)利用圖示實驗裝置進行實驗,實驗步驟如下:檢查裝置氣密性后裝入藥品;打開分液漏斗活塞,_____________________(請按正確的順序填入下列步驟的序號)。
①加熱反應一段時間 ②收集氣體并檢驗其純度
③關閉分液漏斗活塞 ④停止加熱,充分冷卻
(3)裝置B的作用是:_____________________________________;為了確認進入裝置C的氫氣已經干燥,應在B、C之間再接一裝置,該裝置中加入的試劑是:_____________。
(10分,每空2分)
(1)CaH2+2H2O=Ca(OH)2+H2↑ 1︰1
(2)②①④③
(3)除去氫氣中的水蒸氣;無水硫酸銅
【解析】
試題分析:(1)根據題中信息:氫化鈣要密封保存,一旦接觸到水就發生反應生成氫氧化鈣和氫氣,可寫出反應方程式CaH2+2H2O=Ca(OH)2+H2↑;CaH2中H是-1價,Ca(OH)2中H是+1價,是氧化產物;H2中H是0價,是還原產物,氧化產物與還原產物的物質的量之比等于化學計量數之比,是1:1。(2)有氣體參加加熱或燃燒的反應需要首先驗純,實驗完畢后先熄火、冷卻,在停止氣體生成,防止倒吸發生爆炸。(3)H2在發生加熱反應之前需要干燥,一般用無水氯化鈣;檢驗是否干燥用無水硫酸銅,因為無水硫酸銅遇水變藍色現象很明顯。
考點:化學實驗
點評:分析好題中的信息,本題測重基本實驗操作能力考查。


科目:高中化學 來源: 題型:閱讀理解

查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

查看答案和解析>>
科目:高中化學 來源:2012-2013學年山東省魚臺一中高一上學期期末模擬化學試卷(帶解析) 題型:實驗題
(10分)氫化鈣(CaH2,其中H元素的化合價為 –1價)固體是登山運動員常用的能源提供劑。氫化鈣要密封保存,一旦接觸到水就發生反應生成氫氧化鈣和氫氣。氫化鈣通常用氫氣與金屬鈣加熱制取,下圖是模擬制取裝置。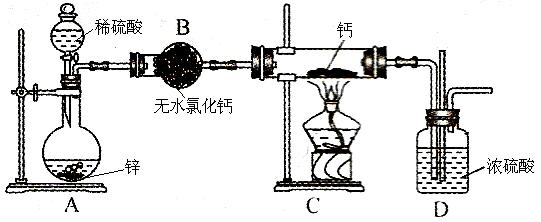
(1)氫化鈣與水反應的化學方程式為:__________________。
該反應中氧化產物與還原產物的物質的量之比為:__________________。
(2)利用圖示實驗裝置進行實驗,實驗步驟如下:檢查裝置氣密性后裝入藥品;打開分液漏斗活塞,_____________________(請按正確的順序填入下列步驟的序號)。
①加熱反應一段時間 ②收集氣體并檢驗其純度
③關閉分液漏斗活塞 ④停止加熱,充分冷卻
(3)裝置B的作用是:_____________________________________;為了確認進入裝置C的氫氣已經干燥,應在B、C之間再接一裝置,該裝置中加入的試劑是:_____________。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年江西省高三高考模擬理綜化學試卷(解析版) 題型:實驗題
氫化鈣(CaH2)固體是登山運動員常用的能源提供劑。氫化鈣要密封保存,一旦接觸到水就發生反應生成氫氧化鈣和氫氣。氫化鈣通常用氫氣與金屬鈣加熱制取,圖1是模擬制取裝置:
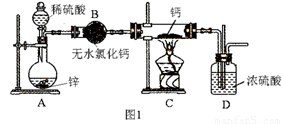
(1)裝置B的作用是 ;裝置D的作用是 ;
(2)利用圖1實驗裝置進行實驗,實驗步驟如下:檢查裝置氣密性后裝入藥品;打開分液漏斗活塞, (請按正確的順序填入下列步驟的序號)。
①加熱反應一段時間 ②收集氣體并檢驗其純度
③關閉分液漏斗活塞 ④停止加熱,充分冷卻
(3)為了確認進入裝置C的氫氣已經干燥,應在B、C之間再接一裝置,該裝置中加入的試劑是: 。
(4)甲同學設計一個實驗,測定上述實驗中得到的氫化鈣的純度(雜質中不含鈣元素。請完善下列實驗步驟:
①樣品稱量;②加入________溶液(填化學式),攪拌、過濾;③________(填操作名稱);④_______ (填操作名稱); ⑤稱量碳酸鈣。
(5)乙同學利用注射器測量氫化鈣和水反應氫氣體積的方法,測定上述實驗中得到的氫化鈣的純度。他稱取46 mg 所制得的氫化鈣樣品,記錄開始時注射器活栓停留在10.00mL刻度處,反應結束后充分冷卻,活栓最終停留在57.04mL刻度處(上述氣體體積均在標準狀況下測定)。試通過計算求樣品中氫化鈣的純度: 。
(6)請你再設計一種氫化鈣純度的測定方法: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com