
| 溫度范圍/℃ | 固體質量/g |
| 258~680 | 3.20 |
| 680~1000 | 1.60 |
| 1000以上 | 1.44 |
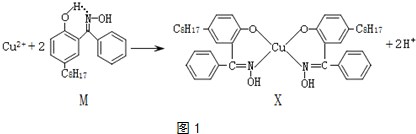
分析 (1)依據X的結構簡式判斷其晶體類型;
(2)元素的非金屬性越強,電負性越強;即同周期自左而右電負性增大;同一主族元素從上到下電負性逐漸減小;
(3)由結構簡式可知X分子中存在配位鍵和共價鍵,據此解答即可;
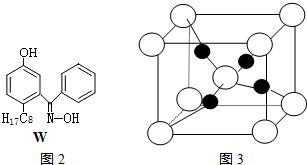
(4)分子內氫鍵的存在,導致水溶性減小,據此解答即可;
(5)①由圖可知,只含有2種原子,則為Cu和O,其化學式為Cu2O,根據硫酸銅的質量計算出物質的量,再求出Cu2O的質量,由固體的質量判斷溫度;
②由圖可知Cu的配位數為4.
解答 解:(1)依據所給X的結構簡式判斷,X難溶于水、易溶于有機溶劑,故X為分子晶體,
故答案為:分子晶體;
(2)化合物X中苯環C和羰基C以sp2雜化,以sp3雜化方式的原子有O、N、C,由于N原子2p軌道半充滿,第一電離能高于O,第一電離能由大到小順序為:N>O>C,
故答案為:N>O>C;
(3)由結構簡式可知X分子中存在配位鍵和共價鍵,
故答案為:be;
(4)由于M能形成分子內氫鍵,導致其溶解度減小,
故答案為:M能形成分子內氫鍵,使溶解度減小;
(5)①由圖可知,只含有2種原子,則為Cu和O,該晶胞中O原子數為1+8×$\frac{1}{8}$=2,Cu原子數為4,其化學式為Cu2O,硫酸銅的物質的量=$\frac{5.00g}{250g/mol}$=0.02mol,氧化亞銅的質量=0.01mol×144g/mol=1.44g,所以加熱溫度在1000℃以上,故答案為:1000℃以上;
②由圖可知Cu的配位數為4;故答案為:4.
點評 本題考查較為綜合,涉及晶體的判斷、電負性比較、氫鍵、化學鍵、計算等知識,題目難度中等,注意掌握均攤法在晶胞計算中的應用,試題知識點較多、綜合性較強,充分考查了學生的分析、理解能力及靈活應用能力.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化學 來源: 題型:選擇題
| 化學式 | 電離常數 |
| HF | Ki=3.5×10-4 |
| H2CO3 | Ki1=4.4×10-7 |
| Ki2=4.7×10-11 | |
| HClO | Ki=3.2×10-8 |
| A. | 同溫同濃度下,溶液的pH:NaF>NaClO>Na2CO3 | |
| B. | 結合H+的能力:ClO-<HCO3-<F- | |
| C. | 次氯酸鈉溶液中通少量二氧化碳的離子方程式:ClO-+CO2+H2O═HCO3-+HClO | |
| D. | 碳酸鈉溶液中加入少量氫氟酸的離子方程式:CO32-+2HF═2F-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
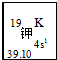 我國的四大發明之一黑火藥,爆炸時反應的化學方程式為:S+2KNO3+3C→K2S+3CO2↑+N2↑.請根據其中所含的元素回答下列問題:
我國的四大發明之一黑火藥,爆炸時反應的化學方程式為:S+2KNO3+3C→K2S+3CO2↑+N2↑.請根據其中所含的元素回答下列問題: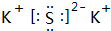 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
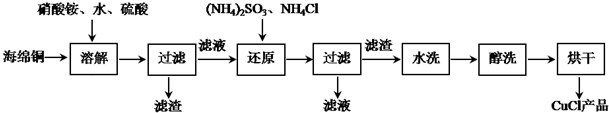
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

| 金 屬 | 熔點(℃) | 沸點(℃) |
| 鈣 | 841 | 1 487 |
| 鑭 | 920 | 3 470 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
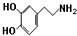 .
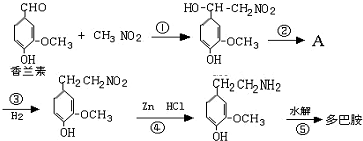
.
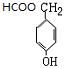
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用酸性高錳酸鉀溶液區別乙烷和乙烯 | |
| B. | 用BaCl2除去NaOH 溶液中混有的少量Na2SO4 | |
| C. | 用KSCN溶液檢驗溶液中含有的Fe2+ | |
| D. | 用溶解、過濾的方法分離CaCl2和NaCl固體混合物 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com