
| 容器 | 溫度/K | 起始物質的量/mol | 平衡物質的量/mol | 平衡常數 | |
| CO2 | H2S | H2O | |||
| Ⅰ | 607 | 0.1 | 0.15 | 0.05 | - |
| Ⅱ | 607 | 0.2 | 0.3 | - | |
| Ⅲ | 627 | 0.1 | 0.15 | - | 6×10-2 |
| A. | 該反應為吸熱反應 | |
| B. | 607K時,該反應的平衡常數為0.50 | |
| C. | 容器Ⅱ達到平衡時,容器中COS的物質的量濃度為0.025 mol.L-1 | |
| D. | 容器Ⅲ達到平衡時,再充入少量氦氣,平衡將向正反應方向移動 |
分析 A.根據三段式列式計算607K時的平衡常數,結合溫度變化和化學平衡常數之間的關機確定反應的吸放熱情況;
B.根據三行式計算607K時平衡常數的大小;
C.根據前兩組實驗,體積不變,初始投料增加1倍,則達到平衡時各物質的物質的量加倍,再根據c=$\frac{n}{V}$計算器濃度;
D.根據濃度對平衡移動的影響來判斷平衡的而移動方向.
解答 解:A.CO2(g)+H2S(g)?COS(g)+H2O(g)
初始量:0.1 0.15 0 0
變化量:0.05 0.05 0.05 0.05
平衡量:0.05 0.1 0.05 0.05
反應前后系數和相等,所以此時K=$\frac{c(COS)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2}S)}$=$\frac{0.05×0.05}{0.05×0.1}$=0.05<6×10-2,溫度升高,K增大,所以反應是吸熱的過程,故A錯誤;
B.根據A的計算可知,607K時該反應的平衡常數為0.5,故B正確;
C.該反應前后氣體體積相等,則壓強不影響平衡,前兩組實驗的體積不變,初始投料增加1倍,則達到平衡時各物質的物質的量加倍,Ⅱ達到平衡時容器中COS的物質的量為0.1mol,濃度為:$\frac{0.1mol}{2L}$=0.05mol/L,故C錯誤;
D.容器Ⅲ達平衡時,再充入少量氦氣,各物質的濃度不變,所以平衡不移動,故D錯誤;
故選B.
點評 本題考查化學平衡的計算,題目難度中等,涉及化學平衡的計算、等效平衡的應用及化學平衡移動原理的應用等知識,注意掌握三段式在化學平衡計算中的應用方法,試題培養了學生的分析能力及化學計算能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
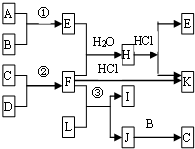 如圖是部分短周期元素的單質及其化合物的轉化關系圖
如圖是部分短周期元素的單質及其化合物的轉化關系圖| 溶液酸堿性 | 離子濃度大小順序 | |
| 1 | 酸性 | |
| 2 | 中性 | |
| 3 | 堿性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 根據碳酸鹽與鹽酸反應能放出二氧化碳氣體,確定某礦石中是否含碳酸鹽 | |
| B. | 根據纖維在火焰上燃燒產生的氣味,確定該纖維是否為蛋白質纖維 | |
| C. | 根據加入氯化鋇溶液的方法來檢驗溶液中是否含有硫酸根離子 | |
| D. | 根據氨氣能使濕潤的紅色石蕊試紙變藍色,可以用于銨根離子的檢驗 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
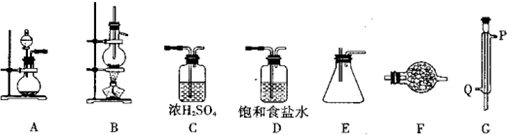
| 密度/(g•cm-3) | 熔點/℃ | 沸點/℃ | |
| 四氯化錫 | 2.2 | -33 | 114 |
| 金屬錫 | 5.77 | 231 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 [Al(OH)2]++H+.
[Al(OH)2]++H+.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④②⑤③ | B. | ⑤②①④③ | C. | ②⑤④①③ | D. | ④①②⑤③ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com