
| A�� | 2molSO2��g����1molO2��g�������еă���С��2molSO3��g�������еă��� | |
| B�� | ��2molSO2��g����1molO2��g������һ���]�����г�ַ�����ų�QkJ�ğ��� | |
| C�� | ���ߜضȣ�ƽ�����淴���Ƅӣ������ữ�W����ʽ�е�Qֵ�pС | |
| D�� | �猢һ����SO2��g����O2��g������ij���]�����г�ַ�����ş�QkJ���t���^������2molSO2��g�������� |
���� A��2SO2��g��+O2��g��?2SO3��g����H=QkJ•mol-1�����ǻ��Ϸ������Ƿşᷴ�������Дࣻ
B�������ǿ��淴���������M����ȫ��
C���ữ�W����ʽ����׃ֻ�c����ϵ�������ȣ��cƽ���Ƅӟo�P��
D��������׃�Y�ϟữ�W����ʽӋ���Д࣮
��� �⣺A�������Ƿşᷴ������ͬ�l���£�2molSO2��g����1molO2��g�������е���������2molSO3��g�������е���������A�e�`��
B����2molSO2��g����1molO2��g������һ���]�����г�ַ������_�����Wƽ�⣬�����ﲻ��ȫ���D�����ų�����С��QkJ����B�e�`��
C�������Ƿşᷴ�������ߜضȣ��mȻԓƽ�����淴�������Ƅӣ����ǟữ�W����ʽ����׃ֻ�c����ϵ�������ȣ��cƽ���Ƅӟo�P�����������ữ�W����ʽ�е�Qֵ��׃����C�e�`��
D���猢һ����SO2��g����O2��g������ij���]�����г�ַ�����ş�QkJ�����ӷ����Ķ��������2mol����һ����2molSO2��g������������D���_��
���xD��
�c�u ���}�����˟ữ�W����ʽ�đ��á����Wƽ���Ӱ����صȣ��P�I�ǿ��淴������׃�����x���⣬�}Ŀ�y���еȣ�


 �����n��ϵ�д�
�����n��ϵ�д� ����˼�S����Ӗ���n�r���W��ϵ�д�
����˼�S����Ӗ���n�r���W��ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
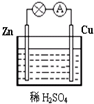 ��1��Zn�O��ԭ늳ص�ؓ���������ؓ�����O��ԓ�O��늘O����ʽ��Zn-2e-=Zn2+�����������������������������߀ԭ����������Cu�O��늘O����ʽ��2H++2e-=H2����
��1��Zn�O��ԭ늳ص�ؓ���������ؓ�����O��ԓ�O��늘O����ʽ��Zn-2e-=Zn2+�����������������������������߀ԭ����������Cu�O��늘O����ʽ��2H++2e-=H2�����鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}

| ���| | Fe��OH��3 | Fe��OH��2 | Zn��OH��2 | Mn��OH��2/Mn��OH��3 |
| �_ʼ����pH | 2.7 | 7.6 | 5.7 | 8.3 |
| ��ȫ����pH ��c��1.0��10-5mol/L�� | 3.7 | 9.6 | 8.0 | 8.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
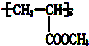 ���@�N���ĽY����ʽ�飨������
���@�N���ĽY����ʽ�飨������| A�� | CH2�TCHCH2OH | B�� | CH3CH2OH | C�� | CH3CH��OH��CH2OH | D�� | CH2ClCHClCH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}

| A�� | ���O������Ag-e-=Ag+ | |
| B�� | ��늕r�����QĤ�����Һ���д�����ɫ�������� | |
| C�� | ���·���D��0.1mole-�r��ͨ�^���QĤ����x�Ӟ�0.2mol | |
| D�� | ��KCl��Һ�����}�ᣬ�t늳ؿ���������׃ |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
| ���� | ������ӷ��� | 늉�/V |
| Fe | Fe��Cu | +0.78 |
| Zn | Zn��Cu | +1.10 |
| A | A��Cu | -0.15 |
| B | B��Cu | +0.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | CH3CH2CHO | B�� | 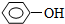 | C�� | CH2=CH2 | D�� | HOOCCH=CH2 |
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com