
| A. | 加入鹽酸以除去硫酸鈉中少量的碳酸鈉雜質 | |
| B. | 用玻璃棒攪拌漏斗中的液體以加快反應速率 | |
| C. | 用稀硫酸和鋅反應制氫氣時加入少許硫酸銅以加快反應速率 | |
| D. | 在容量瓶中加入一定體積的水,再加入濃硫酸配制準確濃度的稀硫酸 |
分析 A.除雜時不能引進新的雜質;
B.過濾時不能用玻璃棒攪拌;
C.原電池能加快反應速率;
D.容量瓶只能配制一定物質的量濃度溶液,不能稀釋或溶解藥品.
解答 解:A.鹽酸和碳酸鈉反應生成氯化鈉,引進新的雜質,應該用稀硫酸除去硫酸鈉中的少量碳酸鈉,故A錯誤;
B.過濾時不能用玻璃棒攪拌,否則易損壞濾紙,故B錯誤;
C.Zn能置換出Cu,Zn、Cu和稀硫酸構成原電池,加快化學反應速率,故C正確;
D.容量瓶只能配制一定物質的量濃度溶液,不能稀釋或溶解藥品,應該將濃硫酸在燒杯中稀釋,然后冷卻至室溫后再轉移到容量瓶中,故D錯誤;
故選C.
點評 本題考查化學實驗方案評價,為高頻考點,涉及除雜、基本操作、化學反應速率影響因素、溶液配制等知識點,明確實驗原理及基本操作是解本題關鍵,注意操作的規范性及儀器用途,注意除雜時要除去雜質且不能引進新的雜質,易錯選項是D.


科目:高中化學 來源: 題型:選擇題
| A. | 6.4g | B. | 9.6g | C. | 11.2g | D. | 12.8g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向NaAlO2溶液中滴入NaHCO3溶液有白色沉淀,原因是二者可以發生雙水解反應 | |
| B. | 電解精煉銅時,若陰極得到1.204×1024個電子,則陽極質量減少6.4g | |
| C. | 使甲基橙變紅色溶液:Mg2+、K+、SO42-、NO3-能大量共存 | |
| D. | Na2S在空氣中長期放置變渾濁的離子方程式為:2S2-+O2+4H+=2S+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
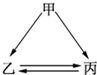 如圖所示的甲、乙、丙三種物質均含有相同的某種元素,箭頭表示物質間的轉化一步就能實現,則甲可能是( )
如圖所示的甲、乙、丙三種物質均含有相同的某種元素,箭頭表示物質間的轉化一步就能實現,則甲可能是( )| A. | ①②③⑤ | B. | ②③④⑤ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.0mol/L的KNO3溶液:H+、Fe2+、SO42- | |
| B. | 強堿性溶液:Na+、HCO3-、NO3-、SO42- | |
| C. | 遇酚酞變紅的溶液中:K+、Na+、NH4+、Br- | |
| D. | 強酸性溶液:Na+、NH4+、SO42-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 生鐵中含有碳,抗腐蝕能力比純鐵強 | |
| B. | 鋼鐵發生析氫腐蝕時,負極反應是:Fe-3e-═Fe3+ | |
| C. | 在鐵制品上鍍銅時,鍍件為陽極,銅鹽為電鍍液 | |
| D. | 鐵管上鑲嵌鋅塊,鐵管不易被腐蝕 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
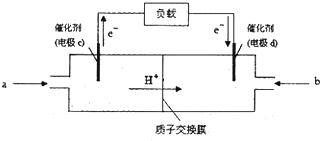
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含有AgCl和AgI固體的懸濁液:c(Ag+)>c(C1-)=c(I-) | |
| B. | CO2的水溶液:c(H+)>c(HCO3-)═2c(CO32-) | |
| C. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)十c(OH-) | |
| D. | 含等物質的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)═2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
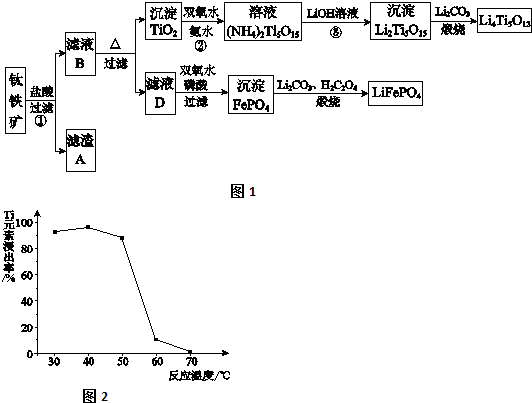
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com