
【選修3物質結構與性質】(15分)
VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表現出多種氧化態,含VIA族元素的化臺物在研究和生產中有許多重要用途。請回答下列問題:
(1)S單質的常見形式為S8,其環狀結構如下圖所示,S原子采用的軌道雜化方式是 ;

(2)原子的第一電離能是指氣態電中性基態原子失去一個電子轉化為氣態基態正離
子所需要的最低能量,O、S、Se原子的第一電離能由大到小的順序為 ;
(3)Se原子序數為 ,其核外M層電子的排布式為 ;
(4)H2Se的酸性比H2S (填“強”或“弱”)。氣態SeO3分子的立體構型
為 ,SO32-離子的立體構型為 ;
(5)H2SeO3的K1和K2分別為2.7x l0-3和2.5x l0-8,H2SeO4第一步幾乎完全電離,
K2為1.2X10-2,請根據結構與性質的關系解釋:
①H2SeO3和H2SeO4第一步電離程度大于第二步電離的原因:
;
② H2SeO4比 H2SeO3酸性強的原因:
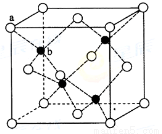
(6)ZnS在熒光體、光導體材料、涂料、顏料等行業中應用廣泛。立方ZnS晶體結構如下圖所示,其晶胞邊長為540.0 pm.密度為 (列式并計算),a位置S2-離子與b位置Zn2+離子之間的距離為 pm(列示表示)
(1)SP3
(2)O>S>Se
(3)34 3s23p63d10
(4)強 正四面體 平面三角形
(5)①H2SeO4和H2SeO3第一步電離產生的氫離子抑制第二步電離,所以第一步電離程度大于第二步電離程度。
②對同一種元素的含鹽酸來說,該元素的化合價越高,其含氧酸的酸性越強。
(6)4.1 
【解析】(1)因為S8為環狀立體結構,鍵角為120°,所以軌道雜化方式為SP3。
(2)根據同主族電離能變化規律,O、S、Se原子的第一電離能由大到小的順序為O>S>Se.(3)Se原子序數為34,其核外M層電子的排布式為3s23p63d10(4)原子半徑越大,氫化物越容易電離出氫離子,所以H2Se的酸性比H2S強。氣態SeO3分子的立體構型為正四面體,SO32-離子的立體構型為平面三角形。(5)①H2SeO4和H2SeO3第一步電離產生的氫離子抑制第二步電離,所以第一步電離程度大于第二步電離程度。

【考點定位】原子的結構與性質、分子的結構與性質、晶體結構與性質、晶體的計算


 通城學典默寫能手系列答案
通城學典默寫能手系列答案 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案科目:高中化學 來源:2013-2014上海市寶山區高二年級化學學科質量監測化學試卷(解析版) 題型:選擇題
明礬[KAl(SO4)2·12H2O]中S元素的化合價是
A. -2 B. +2 C. +4 D. +6
查看答案和解析>>
科目:高中化學 來源:2012年普通高等學校招生全國統一考試化學(海南卷解析版) 題型:簡答題
(9分)
實驗室制備1,2-二溴乙烷的反應原理如下:
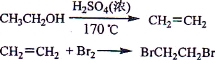
可能存在的主要副反應有:乙醇在濃硫酸的存在下在l40℃脫水生成乙醚。
用少量的溴和足量的乙醇制備1,2—二溴乙烷的裝置如下圖所示:

有關數據列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
狀態 | 色液體 | 無色液體 | 無色液體 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸點/℃ | 78.5 | 132 | 34.6 |
熔點/℃ | 一l30 | 9 | -1l6 |
回答下列問題:
(1)在此制各實驗中,要盡可能迅速地把反應溫度提高到170℃左右,其最主要目的是 ;(填正確選項前的字母)
a.引發反應 b.加快反應速度 c.防止乙醇揮發 d.減少副產物乙醚生成
(2)在裝置C中應加入 ,其目的是吸收反應中可能生成的酸性氣體:(填正確選項前的字母)
a.水 b.濃硫酸 c.氫氧化鈉溶液 d.飽和碳酸氫鈉溶液
(3)判斷該制各反應已經結束的最簡單方法是 ;
(4)將1,2-二溴乙烷粗產品置于分液漏斗中加水,振蕩后靜置,產物應在 層(填“上”、“下”);
(5)若產物中有少量未反應的Br2,最好用 洗滌除去;(填正確選項前的字母)
a.水 b.氫氧化鈉溶液 c.碘化鈉溶液 d.乙醇
(6)若產物中有少量副產物乙醚.可用 的方法除去;
(7)反應過程中應用冷水冷卻裝置D,其主要目的是 ;但又不能過度冷卻(如用冰水),其原因是 。
查看答案和解析>>
科目:高中化學 來源:2012年普通高等學校招生全國統一考試化學(浙江卷解析版) 題型:簡答題
[15分]化合物X是一種環境激素,存在如下轉化關系:
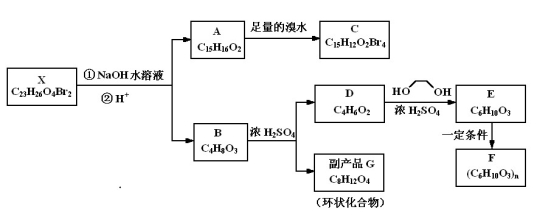
化合物A能與FeCl3溶液發生顯色反應,分子中含有兩個化學環境完全相同的甲基,其苯環上的一硝基取代物只有兩種。1H-NMR譜顯示化合物G的所有氫原子化學環境相同。F是一種可用于制備隱形眼鏡的高聚物。
根據以上信息回答下列問題。
(1)下列敘述正確的是_________。
A.化合物A分子中含有聯苯結構單元
B.化合物A可以和NaHCO3溶液反應,放出CO2氣體
C.X與NaOH溶液反應,理論上1 mol X最多消耗6 mol NaOH
D.化合物D能與Br2發生加成反應
(2)化合物C的結構簡式是_________________,A→C的反應類型是________。
(3)寫出同時滿足下列條件的D的所有同分異構體的結構簡式(不考慮立體異構_________。
a.屬于酯類b.能發生銀鏡反應
(4)寫出B→C反應的化學方程式_______________________________________________。
(5)寫出E→F反應的化學方程式_______________________________________________。
查看答案和解析>>
科目:高中化學 來源:2012年普通高等學校招生全國統一考試化學(浙江卷解析版) 題型:選擇題
以鉻酸鉀為原料,電化學法制備重鉻酸鉀的實驗裝置示意圖如下:
下列說法不正確的是

A.在陰極式,發生的電極反應為:2H2O+2e- 2OH―+H2↑
2OH―+H2↑
B.在陽極室,通電后溶液逐漸由黃色變為橙色,是因為陽極區H+濃度增大,使平衡2 +2H+
+2H+
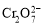 +H2O向右移動
+H2O向右移動
C.該制備過程總反應的化學方程式為:4K2CrO4+4H2O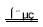 2K2Cr2O7+4KOH+2H2↑+2O2↑
2K2Cr2O7+4KOH+2H2↑+2O2↑
D.測定陽極液中K和Cr的含量,若K與Cr的物質的量之比為d,則此時鉻酸鉀的轉化率為α=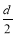
查看答案和解析>>
科目:高中化學 來源:2012年普通高等學校招生全國統一考試化學(新課標解析版) 題型:選擇題
短周期元素W、X、Y、Z的原子序數依次增大,其中W的陰離子的核外電子數與X、Y、Z原子的核外內層電子數相同。X的一種核素在考古時常用來鑒定一些文物的年代,工業上采用液態空氣分餾方法來生產Y的單質,而Z不能形成雙原子分子。根據以上敘述,下列說法中正確的是
A.上述四種元素的原子半徑大小為W<X<Y<Z
B.W、X、Y、Z原子的核外最外層電子數的總和為20
C.W與Y可形成既含極性共價鍵又含非極性共價鍵的化合物
D.由W與X組成的化合物的沸點總低于由W與Y祖傳的化合物的沸點
查看答案和解析>>
科目:高中化學 來源:2012年普通高等學校招生全國統一考試化學(廣東卷解析版) 題型:實驗題
(17分)(2012?廣東)苯甲酸廣泛應用于制藥和化工行業,某同學嘗試用甲苯的氧化反應制備苯甲酸,反應原理:
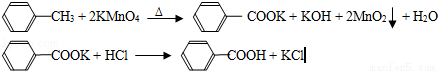
實驗方法:一定量的甲苯和KMnO4溶液在100℃反應一段時間后停止反應,按如下流程分離出苯甲酸和回收未反應的甲苯.
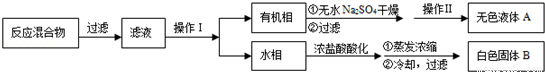
已知:苯甲酸分子量122,熔點122.4℃,在25℃和95℃時溶解度分別為0.3g和6.9g;純凈固體有機物都有固定熔點.
(1)操作Ⅰ為 ,操作Ⅱ為 .
(2)無色液體A是 ,定性檢驗A的試劑是 ,現象是
(3)測定白色固體B的熔點,發現其在115℃開始熔化,達到130℃時仍有少量不熔,該同學推測白色固體B是苯甲酸與KCl的混合物,設計了如下方案進行提純和檢驗,實驗結果表明推測正確.請在答題卡上完成表中內容.
序號 | 實驗方案 | 實驗現象 | 結論 |
① | 將白色固體B加入水中,加熱溶解, _________ _________ | 得到白色晶體和無色溶液 |
|
② | 取少量濾液于試管中, _________ | 生成白色沉淀 | 濾液含Cl﹣ |
③ | 干燥白色晶體, _________ | _________ | 白色晶體是苯甲酸 |
(4)純度測定:稱取1.220g產品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物質的量為2.40×10﹣3mol,產品中苯甲酸質量分數的計算表達式為 ,計算結果為 (保留二位有效數字).
查看答案和解析>>
科目:高中化學 來源:2012年普通高等學校招生全國統一考試化學(山東卷解析版) 題型:填空題
(12分)(2012?山東)工業上由黃銅礦(主要成分CuFeS2)冶煉銅的主要流程如下:

(1)氣體A中的大氣污染物可選用下列試劑中的 吸收.
a.濃H2SO4 b.稀HNO3
c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈紅色,說明溶液中存在 (填離子符號),檢驗溶液中還存在Fe2+的方法是 (注明試劑、現象).
(3)由泡銅冶煉粗銅的化學反應方程式為 .
(4)以CuSO4溶液為電解質溶液進行粗銅(含Al、Zn、Ag、Pt、Au等雜質)的電解精煉,下列說法正確的是 .
a.電能全部轉化為化學能
b.粗銅接電源正極,發生氧化反應
c.溶液中Cu2+向陽極移動
d.利用陽極泥可回收Ag、Pt、Au等金屬
(5)利用反應2Cu+O2+2H2SO4═2CuSO4+2H2O可制備CuSO4,若將該反應設計為原電池,其正極電極反應式為 .
查看答案和解析>>
科目:高中化學 來源:2012-2013陜西省富平縣高一下學期期末考試化學試卷(解析版) 題型:計算題
某含氧有機物的相對分子質量為60,1 mol該有機物完全燃燒,生成36gH2O和44.8L CO2(標準狀況下)。
(1)求該有機物分子式;
(2)又知此有機物具有弱酸性,能與金屬鈉反應,也能與堿溶液反應,試寫出它可能的結構簡式。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com