
資料顯示:鎂與飽和碳酸氫鈉溶液反應產(chǎn)生大量氣體和白色不溶物。某同學設計了如下實驗方案并驗證產(chǎn)物、探究反應原理。
(1)提出假設
實驗I:用砂紙擦去鎂條表面氧化膜,將其放入盛有適量滴有酚酞的飽和碳酸氫鈉溶液的試管中,迅速反應,產(chǎn)生大量氣泡和白色不溶物,溶液由淺紅變紅。
該同學對反應中產(chǎn)生的白色不溶物做出如下猜測:
猜測1:白色不溶物可能為 。
猜測2:白色不溶物可能為MgCO3。
猜測3:白色不溶物可能是堿式碳酸鎂[xMgCO3·yMg(OH)2]。
(2)設計定性實驗確定產(chǎn)物并驗證猜測:
|
實驗序號 |
實驗 |
實驗現(xiàn)象 |
結論 |
|
實驗Ⅱ |
將實驗I中收集到的氣體點燃 |
能安靜燃燒、產(chǎn)生淡藍色火焰 |
氣體成分為______ |
|
實驗Ⅲ |
取實驗I中的白色不溶物,洗滌,加入足量 ‚ |
ƒ |
白色不溶物可能含有MgCO3 |
|
實驗Ⅳ |
取實驗I中的澄清液,向其中加入少量CaCl2稀溶液 |
產(chǎn)生白色沉淀 |
溶液中存在 ④ 離子 |
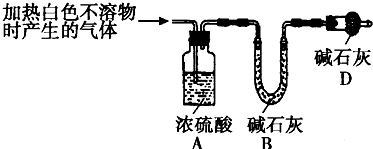
(3)為進一步確定實驗I的產(chǎn)物,設計定量實驗方案,如圖所示:

稱取實驗Ⅰ中所得干燥、純凈的白色不溶物22.6 g,充分加熱至不再產(chǎn)生氣體為止,并使分解產(chǎn)生的氣體全部進入裝置A和B中。實驗前后裝置A增重1.8 g,裝置B增重8.8 g,試確定白色不溶物的化學式 。
(4)請結合化學用語和化學平衡移動原理解釋Mg和NaHCO3溶液反應產(chǎn)生大量氣泡的原因_________。
(共9分)
(1)猜測1:Mg(OH)2 (1分)
(2)①氫氣 ;②稀鹽酸(合理均可);
③ 產(chǎn)生氣泡,沉淀全部溶解 ;④CO2- 3(各1分)
(3) 2MgCO3·Mg(OH)2 或 Mg(OH)2·2MgCO3 或 Mg3(OH)2(CO3)2
(4)NaHCO3溶液中存在如下平衡:HCO- 3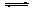 H+ +CO2- 3、H2O
H+ +CO2- 3、H2O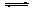 H++OH-;Mg和H+反應生成H2和Mg2+,Mg2+跟OH-、CO32-生成難溶物Mg(OH)2·2MgCO3,則H+、OH-、CO2- 3的濃度均降低,促使上述兩平衡均向右移動。故Mg和飽和NaHCO3溶液反應產(chǎn)生大量氣體H2。
H++OH-;Mg和H+反應生成H2和Mg2+,Mg2+跟OH-、CO32-生成難溶物Mg(OH)2·2MgCO3,則H+、OH-、CO2- 3的濃度均降低,促使上述兩平衡均向右移動。故Mg和飽和NaHCO3溶液反應產(chǎn)生大量氣體H2。
【解析】
試題分析:
(1)由題可知猜測為Mg(OH)2
(2)①鎂與水反應生成氫氣。②檢測碳酸鹽一般加入鹽酸。③看是否有二氧化碳生成。④溶液中有CO32-與Ca2+生成白色沉淀。
(3)根據(jù)題意可得關系式Mg(OH)2~H2O,MgCO3~CO2,n(H2O)=1.8g/18g/mol=0.1mol,n(CO2)=8.8g/44g/mol=0.2mol,可知為2MgCO3·Mg(OH)2 或 Mg(OH)2·2MgCO3 或Mg3(OH)2(CO3)2 。
(4)NaHCO3溶液中存在如下平衡:HCO- 3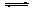 H+
+CO2- 3、H2O
H+
+CO2- 3、H2O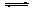 H++OH-;Mg和H+反應生成H2和Mg2+,Mg2+跟OH-、CO32-生成難溶物Mg(OH)2·2MgCO3,則H+、OH-、CO2- 3的濃度均降低,促使上述兩平衡均向右移動。故Mg和飽和NaHCO3溶液反應產(chǎn)生大量氣體H2。
H++OH-;Mg和H+反應生成H2和Mg2+,Mg2+跟OH-、CO32-生成難溶物Mg(OH)2·2MgCO3,則H+、OH-、CO2- 3的濃度均降低,促使上述兩平衡均向右移動。故Mg和飽和NaHCO3溶液反應產(chǎn)生大量氣體H2。
考點:本題以實驗探究為載體考查元素及其化合物性質(zhì)、化學計算等相關知識。。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:閱讀理解
| 實驗序號 | 實驗 | 實驗現(xiàn)象 | 結論 |
| 實驗Ⅱ | 將實驗Ⅰ中收集到的氣體點燃 | 能安靜燃燒、產(chǎn)生淡藍色火焰 | ①氣體成分為 氫氣 氫氣 |
| 實驗Ⅲ | ②取實驗Ⅰ中的白色不溶物,洗滌,加入足量 稀鹽酸 稀鹽酸 |
③ 產(chǎn)生氣泡沉淀全部溶解 產(chǎn)生氣泡沉淀全部溶解 |
白色不溶物可能含有MgCO3 |
| 實驗Ⅳ | 取實驗Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 產(chǎn)生白色沉淀 | ④溶液中存在 CO32- CO32- |

查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 實驗序號 | 實驗 | 實驗現(xiàn)象 | 結論 |
| 實驗Ⅱ | 將實驗Ⅰ中收集到的氣體點燃 | 能安靜燃燒、產(chǎn)生淡藍色火焰 | 氣體成為 ①氫氣 ①氫氣 |
| 實驗Ⅲ | 取實驗Ⅰ中的白色不溶物,洗滌, 加入足量 ②稀鹽酸 ②稀鹽酸 |
③產(chǎn)生氣體沉淀全部溶解 ③產(chǎn)生氣體沉淀全部溶解 |
白色不溶物可能是MgCO3 |
| 實驗Ⅳ | 取實驗Ⅰ中的澄清溶液, 向其中加入少量稀CaCl2溶液 |
產(chǎn)生白色沉淀 | 溶液中存在 ④CO32- ④CO32- |
查看答案和解析>>
科目:高中化學 來源:2013-2014學年安徽省高三上學期期中考試化學試卷(解析版) 題型:實驗題
資料顯示:鎂與飽和碳酸氫鈉溶液反應產(chǎn)生大量氣體和白色不溶物。某同學通過如下實驗探究反應原理并驗證產(chǎn)物。
實驗I:用砂紙擦去鎂條表面氧化膜,將其放入盛適量滴有酚酞的飽和碳酸氫鈉溶液的燒杯中,迅速反應,產(chǎn)生大量氣泡和白色不溶物,溶液的淺紅色加深。
(1)該同學對反應中產(chǎn)生的白色不溶物做出如下猜測:
猜測1:白色不溶物可能為
猜測2:白色不溶物可能為MgCO3
猜測3:白色不溶物可能為堿式碳酸鎂[yMg(OH)2•xMgCO3]
(2)為了確定產(chǎn)物,進行以下定性實驗:
|
實驗序號 |
實 驗 |
實驗現(xiàn)象 |
結 論 |
|
實驗Ⅱ |
將實驗I中收集到的氣體點燃 |
安靜燃燒, 火焰呈淡藍色 |
氣體成分為 ① |
|
實驗Ⅲ |
將實驗I中的白色不溶物濾出、洗滌,取少量加入足量 ② |
③ |
白色不溶物中含有MgCO3 |
|
實驗Ⅳ |
取實驗Ⅲ中的濾液,向其中加入適 量 ④ 稀溶液 |
產(chǎn)生白色沉淀,溶液紅色變淺 |
溶液中存在CO32- 離子 |
實驗Ⅲ中洗滌的操作方法是 。
(3)為進一步確定實驗I的白色不溶物的成分,進行以下定量實驗,裝置如圖所示:

稱取干燥、純凈的白色不溶物 4.52 g,充分加熱至不再產(chǎn)生氣體為止,并使分解產(chǎn)生的氣體全部進入裝置A和B中。實驗后裝置A增重0.36 g,裝置B增重1.76 g。
裝置C的作用是 ;
白色不溶物的化學式為 。
(4)寫出鎂與飽和碳酸氫鈉溶液反應的化學方程式 。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年廣東省梅州市高三總復習質(zhì)檢二理綜化學試卷(解析版) 題型:實驗題
某興趣小組根據(jù)鎂與沸水的反應推測鎂也能與飽和碳酸氫鈉溶液反應。資料顯示:鎂與飽和碳酸氫鈉溶液反應產(chǎn)生大量氣體和白色不溶物。該興趣小組設計了如下實驗方案并驗證產(chǎn)物、探究反應原理。
實驗1:用砂紙擦去鎂條表面氧化膜,將其放人盛有適量滴有酚酞的飽和碳酸氫鈉溶液的試管中,迅速反應,產(chǎn)生大量氣泡和白色不溶物,溶液由淺紅變紅。
(1)提出假設
該同學對反應中產(chǎn)生的白色不溶物作出如下假設:
假設1:可能為 。
假設2:可能為MgCO3。
假設3:可能是堿式碳酸鎂[xMgCO3·yMg(OH)2]
(2)設計定性實驗確定產(chǎn)物并驗證猜測:
|
實驗序號 |
實驗 |
預期現(xiàn)象和結論 |
|
實驗II |
將實驗I中收集到的氣體點燃 |
|
|
實驗III |
取實驗I中的白色不溶物,洗滌,加入足量 |
; 白色不溶物可能含有MgCO3 |
|
實驗IV |
取實驗I中的澄清液,向其中加入少量CaCl2稀溶液 |
產(chǎn)生白色沉淀;溶液中存在 離子 |
(3)設計定量實驗確定實驗I的產(chǎn)物:稱取實驗I中所得干燥、純凈的白色不溶物31.0 g,充分加熱至不再產(chǎn)生氣體為止,并使分解產(chǎn)生的氣體全部進入盛有足量濃硫酸的洗氣瓶A、盛有足量堿石灰的干燥管B和盛有足量堿石灰的干燥管C中。實驗前后裝置A增重1.8 g,裝置B增重13.2 g,試確定白色不溶物的化學式 。
(4)請結合化學用語和化學平衡移動原理解釋Mg和NaHCO3溶液反應產(chǎn)生大量氣泡的原因 。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com