
【題目】在通電條件下,用如圖所示裝置由乙二醛(OHC-CHO)制備乙二酸(H00C-COOH)。其制備反應為:OHC-CHO+2Cl2+2H2O→HOOC-COOH+4HCl。下列說法正確的是

A. 每消耗0.1mol乙二醛在Pt1極放出2.24L氣體(標準狀況)
B. Pt1的電極反應為:4OH--4e-=2H2O+O2↑
C. 每得到lmol乙二酸將有2molH+從右室遷移到左室
D. 鹽酸是起提供Cl-和增強導電性的作用
 優質課堂快樂成長系列答案
優質課堂快樂成長系列答案科目:高中化學 來源: 題型:
【題目】近年來,我國在超導研究方面居世界領先地位,鉈(Tl)是超導體的組成成分之一,鉈位于第6周期ⅢA族,下列對鉈的性質推導可能正確的是( )
①鉈是易導電的銀白色金屬
②Tl(OH)3是兩性氫氧化物
③Tl3+的氧化能力比Al3+的強
④單質能跟稀HNO3反應生成硝酸鹽
A. ①④ B. ②③ C. 只有① D. 只有④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式書寫正確的是( )
A. Na2O2與H2O反應:2![]() +2H2O4OH-+O2↑
+2H2O4OH-+O2↑
B. 金屬鈉投入水中:Na+2H2O=Na++OH-+H2↑
C. CaCO3與醋酸溶液反應:CaCO3+2H+Ca2++CO2↑+H2O
D. KAl(SO4)2溶液與氨水反應:Al3++3NH3·H2OAl(OH)3↓+3N![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按如圖所示裝置進行實驗,以制取乙酸乙酯。
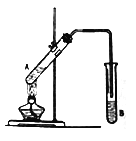
(1)試管A中的液體由以下試劑混合而成:①2mL乙醇;②3mL濃硫酸;③2mL 乙酸。一般況下,這三種試劑的加入順序是:先加入________(填序號,下同),再加入_________,最后加入③。
(2)為防止試管A中的液體在實驗時發生暴沸,在加熱前還應加入碎瓷片。若加熱后發現未加入碎瓷片,應采取的補救措施是:_________________________________________________________。
(3)試管B中盛放的試劑是___________________;反應結束后,分離B中的液體混合物需要用到的玻璃儀器主要是_____________。試管B中的導管末端不伸入液面下方的目的是_______________。
(4)試管 A中CH3COOH與C2H518OH反應的化學方程式為:___________________________________。
(5)該實驗中用30gCH3COOH與46gC2H5OH反應,如果實際得到的乙酸乙酯的質量是26.4g,該實驗中乙酸乙酯的產率是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子中,因發生氧化還原反應而不能大量共存的是
A. K+、H+、Fe2+、MnO4-B. Fe3+、Ba2+、SO42-、NO3-
C. Al3+、Na+、SO42-、CO32-D. Fe3+、H+、SO42-、ClO-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中不正確的是( )
A. 化石燃料在任何條件下都能充分燃燒
B. 化石燃料在燃燒過程中能產生污染環境的CO、SO2等有害氣體
C. 直接燃燒煤不如將煤進行深加工后,再燃燒效果好
D. 固體煤變為氣體燃料后,燃燒效率將更低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中不能得到氫氧化鋁沉淀的是 ( )
A. 硫酸鋁溶液與過量的氨水混合B. 氯化鋁溶液中加入幾滴燒堿溶液
C. 偏鋁酸鈉溶液中加入過量的鹽酸D. 偏鋁酸鈉溶液中通入過量的二氧化碳
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵及其化合物在生產和生活中有廣泛的應用。
Ⅰ、高鐵酸鈉(Na2FeO4)是一種新型凈水劑,工業上制備高鐵酸鈉的反應原理為:
Fe(OH)3 + NaClO + NaOH →Na2FeO4 + X + H2O(未配平), 則X的電子式為_______ ,反應中被氧化的物質是_________(寫化學式)。
Ⅱ、鐵紅顏料跟某些油料混合,可以制成防銹油漆。工業制硫酸產生的硫酸渣中主要含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制備鐵紅(Fe2O3)的過程如下:
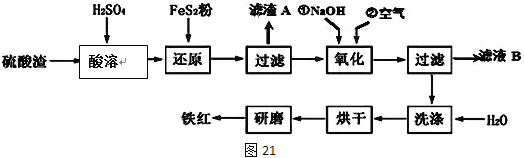
已知:
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
開始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
已知FeS2是一種黃色難溶于水的固體。
(1)酸溶過程中Fe2O3與稀硫酸反應的化學方程式為______________________;
“濾渣A”主要成份的化學式為__________________。
(2)還原過程中加入FeS2的目的是將溶液中的Fe3+還原為Fe2+,而本身被氧化為H2SO4,寫出該反應的離子方程式_________________。
(3)為確保鐵紅的質量和純度,氧化過程中加NaOH調節溶液pH的范圍是____;如果加NaOH調節溶液pH=a,則濾液B中c(Fe3+)=____mol/L(25℃時,Ksp[Fe(OH)3]=4×10﹣38)
(4)以甲醚、空氣、氫氧化鉀溶液為原料,石墨為電極可以構成燃料電池。該電池負極的電極反應式為________________ 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com