
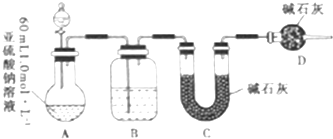
分析 裝置A中的亞硫酸鈉加入濃硫酸反應生成二氧化硫氣體,通過裝置B中濃硫酸干燥氣體,用裝置C吸收二氧化硫,裝置D是防止空氣中的水蒸氣和二氧化碳干擾二氧化硫氣體質量的測定,
(1)根據濃鹽酸、濃硝酸和濃硫酸的性質判斷應選取的物質;
(2)堿石灰能吸收二氧化硫,所以C裝置增重的質量就是二氧化硫的質量,根據二氧化硫的質量計算亞硫酸鈉固體中含有的亞硫酸鈉,從而計算出其濃度;
(3)二氧化硫能儲存在某些裝置中.
解答 解:(1)A、濃硝酸有揮發性,且濃硝酸有強氧化性,能把亞硫酸根離子氧化成硫酸根離子而得不到二氧化硫氣體,故A錯誤;
B、稀硫酸的氧化性是氫元素表現,反應速率較慢,濃硫酸主要以分子存在,而亞硫酸鈉和硫酸的反應是在溶液中以離子進行反應,所以用65%硫酸和亞硫酸鈉固體反應制取二氧化硫,故B正確;
C、濃鹽酸有揮發性,會對實驗造成干擾,故C錯誤,
故答案為:B;
(2)堿石灰能吸收二氧化硫,所以C裝置增重的質量就是二氧化硫的質量,
設亞硫酸鈉的物質的量濃度為C,
H2SO4+Na2SO3=H2O+Na2SO4+SO2↑
1mol 64g
0.06Cmol 3.2g
C=0.83mol•L-1,
故答案為:0.83;
(3)二氧化硫能儲存在某些裝置中導致堿石灰吸收的二氧化硫減少,造成偏差,所以存在的缺陷是:缺少一個驅趕殘留二氧化硫氣體的裝置,
故答案為:缺少一個驅趕殘留二氧化硫氣體的裝置.
點評 本題考查了亞硫酸鈉漂白性的探究實驗,難度不大,注意實驗室制取二氧化硫時選取的酸不能是濃鹽酸、濃硝酸和98%的濃硫酸.


科目:高中化學 來源: 題型:選擇題

| A. | 當n=1時,X可能是C | B. | 當n=1時,X可能是Al | ||
| C. | 當n=2時,X可能是S | D. | 當n=2時,X可能是Na |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向稀HNO3中滴加Na2SO3溶液:2H++SO32-═SO2↑+H2O | |
| B. | 向Al2(SO4)3溶液中加入過量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| C. | 用高錳酸鉀標準溶液滴定草酸:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O | |
| D. | 向0.1mol/LpH=1的KHA溶液中加入KOH溶液:H++OH-═H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 現象 | 結論 |
| A | 將少量某物質的溶液滴加到新制氫氧化銅中,加熱 | 有紅色沉淀生成 | 該物質一定屬于醛類 |
| B | 向AgNO3溶液中滴加過量氨水 | 溶液澄清 | Ag+與NH3•H2O能大量共存 |
| C | 將某氣體通入品紅溶液中 | 品紅溶液褪色 | 該氣體一定是SO2 |
| D | 將0.1mol/L MgSO4溶液滴入NaOH溶液至不再有沉淀產生,再滴加0.1mol/L CuSO4溶液 | 先有白色沉淀生成后變為淺藍色沉淀 | Cu(OH)2的溶解度小于Mg(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
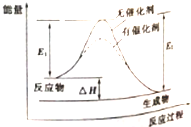
| A. | 該反應能量變化類型與CaCO3分解反應相同 | |
| B. | 加催化劑后,正反應速率加快,逆反應速率減小 | |
| C. | 若該反應為氧化還原反應,則可以將其設計成原電池 | |
| D. | 反應熱△H=E2-E1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑由大到小的順序為Z>X>Y | |
| B. | Z元素的氫化物是一種強酸 | |
| C. | 元素非金屬性由強到弱的順序為X>Y>Z | |
| D. | 3種元素的氣態氫化物中,Y的氣態氫化物還原性最強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
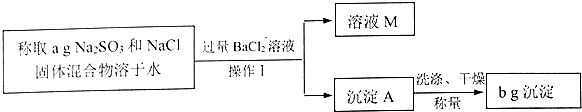
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com