
分析 A.滴定時,眼睛應始終注視錐形瓶內液體顏色變化;
B.滴定實驗不一定都需要指示劑;
C.酸堿中和滴定之前,錐形瓶用蒸餾水洗凈即可,不能用待測液潤洗,否則會導致測定值偏大;
D.用pH試紙測量某溶液的pH時不能先將試紙潤濕,否則有偏差;
E.滴定管經蒸餾水洗凈后,直接注入標準液,會導致標準液濃度偏低;
F.泛pH試紙測定值為整數;
G.滴定終點附近間隔要小些.
解答 解:A.酸堿中和滴定實驗中,滴定時眼睛注視錐形瓶中溶液的顏色變化,以便及時判斷滴定終點,不需要觀察滴定管內液面的變化,故A錯誤;
B.KMnO4本身為紫紅色,則用KMnO4滴定亞硫酸鈉溶液的實驗到達終點時,將出現紅色,所以不需要另外加入指示劑,故B錯誤;
C.錐形瓶用蒸餾水洗凈后,又用待測溶液潤洗,增大待測液中的溶質的物質的量,消耗標準液體積增大,測定結果偏大,故C正確;
D.用pH試紙測量某溶液的pH時將試紙潤濕,則溶液被稀釋,影響測定結果,故D錯誤;
E.滴定管洗凈后經蒸餾水潤洗,即可注入標準液進行滴定,標準液濃度降低,消耗標準液體積增大,測定結果偏大,故E正確;
F.泛pH試紙測定值為整數,所以讀數不可能是小數,故F錯誤;
G.滴定終點附近間隔要小些,否則可能產生較大誤差,故G錯誤;
故選CE.
點評 本題考查化學實驗方案評價,為高頻考點,側重考查學生分析判斷、實驗操作及實驗評價能力,明確實驗原理、實驗操作方法是解本題關鍵,易錯選項是B.


 口算題天天練系列答案
口算題天天練系列答案科目:高中化學 來源: 題型:解答題
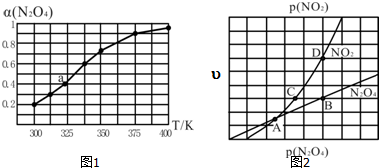
| 化學鍵 | N-H | N-N | N≡N | O-H |
| E/(kJ•mol-1) | 390 | 190 | 946 | 460 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 都能使溶液的pH增大 | |
| B. | 都能使溶液中c(H+)•c(CH3COO-)減小 | |
| C. | 都能使溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$比值增大 | |
| D. | 溶液中$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 工業上有一種用C02來生產甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,將6mol CO2和8mol H2充入2L的密閉容器中,測得H2的物質的量隨時間變化如圖所示(實線).圖中數據a(1,6)表示:在1min時H2的物質的量是6mol.
工業上有一種用C02來生產甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,將6mol CO2和8mol H2充入2L的密閉容器中,測得H2的物質的量隨時間變化如圖所示(實線).圖中數據a(1,6)表示:在1min時H2的物質的量是6mol.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 僅在高溫下 | B. | 在任何溫度下都不能自發進行 | ||
| C. | 在任何溫度下 | D. | 僅在低溫下 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com