
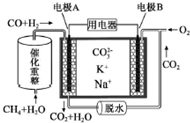
| A. | 反應CH4+H2O$\frac{\underline{\;催化劑\;}}{△}$3H2+CO,每消耗1molCH4轉移6mol 電子 | |
| B. | 電極A上CO參與的電極反應為:CO+CO32--2e-═2CO2↑ | |
| C. | 電池工作時,CO32-向電極B移動 | |
| D. | 電極B上發生的電極反應為:O2+2CO2+4e-═2CO32- |
分析 A.根據C元素的化合價變化分析;
B.CO在負極上失電子生成二氧化碳;
C.原電池中陰離子向負極移動;
D.電極B上氧氣得電子發生還原反應.
解答 解:A.反應CH4+H2O$\frac{\underline{\;催化劑\;}}{△}$3H2+CO中,1molCH4→CO,化合價由-4價→+2,上升6價,則1molCH4參加反應共轉移6mol電子,故A正確;
B.CO在負極上失電子生成二氧化碳,則電極A上CO參與的電極反應為:CO+CO32--2e-═2CO2↑,故B正確;
C.原電池中陰離子向負極移動,A通入燃料,則A為負極,所以CO32-向電極A移動,故C錯誤;
D.電極B上氧氣得電子發生還原反應,則電極B上發生的電極反應為:O2+2CO2+4e-═2CO32-,故D正確.
故選C.
點評 本題考查了化學電源新型電池,明確原電池中物質得失電子、電子流向、離子流向即可解答,題目難度不大,側重于考查學生的分析能力和對基礎知識的應用能力.


科目:高中化學 來源: 題型:選擇題
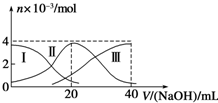
| A. | 等濃度的NaOH溶液與H2A溶液按2:1混合后,其溶液中水的電離程度比純水大 | |
| B. | 當V(NaOH)=20 mL時,溶液中離子濃度大小關系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) | |
| C. | NaHA溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A) | |
| D. | 向上述加入20mLNaOH溶液后所得溶液中再加入水的過程中,pH可能減少 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分別用H2O2、KMnO4分解制O2,當制得等質量O2時,轉移電子數之比為1:2 | |
| B. | 等質量的O2與O3中,氧原子的個數比為3:2 | |
| C. | CaCl2及CaO2固體中陰、陽離子數之比均為2:1 | |
| D. | 10mL 0.3mol/LNaCl與30mL0.1mol/LAlCl3溶液中Cl-物質的量濃度比為1:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 天津港爆炸案中對劇毒的氰化鈉(NaCN) 噴灑雙氧水消毒,是利用了雙氧水的氧化性 | |
| B. | 碳酸鈣分解、氫氧化鋇晶體和氯化銨固體反應、高溫下鋁與氧化鐵反應都是吸熱反應 | |
| C. | 瑪瑙的主要成分是二氧化硅,陶瓷的主要成分是硅酸鹽 | |
| D. | 豆漿制豆腐、納米材料、塑料、橡膠及合成纖維等制造過程都會用到膠體的性質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 屠呦呦女士利用乙醚萃取青蒿素獲得了2015年度諾貝爾生理學或醫學獎,為人類防治瘧疾作出了重大貢獻 | |
| B. | 光導纖維應避免在強堿性環境中使用 | |
| C. | 硅膠多孔、吸水能力強,常用作袋裝食品的干燥 | |
| D. | 陶瓷、水泥、玻璃、大理石屬于硅酸鹽產品 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
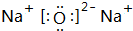 、
、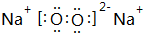 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com