
分析 (1)HCl是強電解質,故0.1mol/L的鹽酸溶液中,c(H+)=0.1mol/L,根據水的離子積求出溶液中c(OH-),而溶液中的氫氧根全部來自于水的電離,且水電離出的c(H+)=c(OH-),據此分析計算;
(2)100℃時,Kw=10-12,NaOH溶液中,氫氧根基本全部來自于氫氧化鈉本身,故可知0.1mol/L的氫氧化鈉溶液中c(OH-),繼而可求出溶液中的c(H+),而溶液中的氫離子全部來自于水,且水電離出的c(H+)=c(OH-),據此分析計算.
解答 解:(1)HCl是強電解質,故0.1mol/L的鹽酸溶液中,c(H+)=0.1mol/L,根據水的離子積求出溶液中c(OH-)=$\frac{1{0}^{-14}}{0.1}$=10-13mol/L,而溶液中的氫氧根全部來自于水的電離,且水電離出的c(H+)=c(OH-)=10-13mol/L,故答案為:0.1mol/L;10-13mol/L;10-13mol/L;
(2)100℃時,Kw=10-12,NaOH溶液中,氫氧根基本全部來自于氫氧化鈉本身,故可知0.1mol/L的氫氧化鈉溶液中c(OH-)=0.1mol/L,故溶液中的c(H+)=$\frac{1{0}^{-12}}{0.1}$=10-11mol/L,而溶液中的氫離子全部來自于水,且水電離出的c(H+)=c(OH-)=10-11mol/L,
故答案為:0.1mol/L;10-11mol/L;10-11mol/L.
點評 本題考查酸堿溶液中pH的相關計算,注意100℃時Kw=10-12,明確由水電離出的c(H+)=c(OH-)是解答本題的關鍵,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:多選題
| A. | 混合氣體中一定含有甲烷 | B. | 混合氣體一定是甲烷和乙烯 | ||
| C. | 混合氣體中一定含有乙烷 | D. | 混合氣體可能是甲烷和乙烯 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
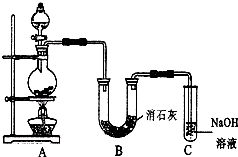 某學生設計如圖所示的實驗裝置,利用氯氣與潮濕的消石灰反應制取少量漂白粉(這是一個放熱反應).
某學生設計如圖所示的實驗裝置,利用氯氣與潮濕的消石灰反應制取少量漂白粉(這是一個放熱反應).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (苯甲醛)+(CH3CO)2O(乙酸酐)$→_{140-170℃}^{K_{2}CO_{3}}$
(苯甲醛)+(CH3CO)2O(乙酸酐)$→_{140-170℃}^{K_{2}CO_{3}}$ (肉桂酸)+CH3COOH(乙酸)
(肉桂酸)+CH3COOH(乙酸)| 名稱 | 分子量 | 性狀 | 密度g/cm3 | 熔點℃ | 沸點℃ | 溶解度:克/100ml溶劑 | ||
| 水 | 醇 | 醚 | ||||||
| 苯甲醛 | 106 | 無色液體 | 1.06 | -26 | 178-179 | 0.3 | 互溶 | 互溶 |
| 乙酸酐 | 102 | 無色液體 | 1.082 | -73 | 138-140 | 12 | 溶 | 不溶 |
| 肉桂酸 | 148 | 無色結晶 | 1.248 | 133-134 | 300 | 0.04 | 24 | 溶 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com