
| 化學式 | 電離常數 |
| CH3COOH | K=1.7×10-5 |
| HCN | K=4.9×10-10 |
| H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |
| A. | H2CO3、HCO3-、CH3COO-、CN- | B. | HCO3-、CH3COOH、CN-、CO32- | ||
| C. | HCN、HCO3-、CN-、CO32- | D. | HCN、HCO3-、CH3COO-、CN- |
分析 電離平衡常數越大酸性越強,根據電離平衡常數可知,酸性強弱為:CH3COOH>H2CO3>HCN>HCO3-,
A.四種離子之間不反應,能夠共存;
B.醋酸能夠與其它三種離子發生反應;
C.HCN能夠與碳酸根離子反應生成碳酸氫根離子;
D.四種離子之間不發生反應,能夠共存.
解答 解:電離平衡常數越大酸性越強,根據電離平衡常數可知,酸性強弱為:CH3COOH>H2CO3>HCN>HCO3-,
A.H2CO3、HCO3-、CH3COO-、CN-之間不反應,能夠大量共存,故A正確;
B.酸性CH3COOH>H2CO3>HCN>HCO3-,CH3COOH與HCO3-、CN-、CO32-發生反應,在溶液中不能大量共存,故B錯誤;
C.酸性HCN>HCO3-,HCN、HCO3-之間發生反應,在溶液中不能大量共存,故C錯誤;
D.HCN、HCO3-、CH3COO-、CN-之間不反應,在溶液中能夠大量共存,故D正確;
故選AD.
點評 本題考查離子共存的正誤判斷,為高考的高頻題,題目難度不大,正確判斷酸性強弱為解答關鍵;試題側重對學生基礎知識的訓練和檢驗,有利于培養學生的邏輯推理能力,提高學生靈活運用基礎知識解決實際問題的能力.


 ABC考王全優卷系列答案
ABC考王全優卷系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| B | C |
| D |
| A. | 簡單離子的半徑大小關系:C>E | |
| B. | D元素的氣態氫化物比C元素的氣態氫化物穩定 | |
| C. | 由A、B、C三種元素組成的離子化合物中,陰、陽離子個數比為1:1 | |
| D. | 由C、D、E三種元素組成的化合物只有一種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
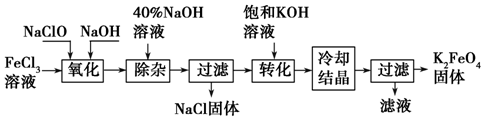
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗 | 現象 |
| A | 加熱放在坩堝中的小鈉塊 | 鈉先熔化成光亮的小球,燃燒時,火焰為黃色,燃燒后,生成淡黃色固體 |
| B | 在酒精燈上加熱鋁箔 | 鋁箔熔化,失去光澤,熔化的鋁并不滴落,好像有一層膜兜著 |
| C | 在含有酚酞的水中加入一小塊鈉 | 鈉浮在水面上,四處游動,發出嘶嘶響聲,溶液變紅 |
| D | 在空氣中久置的鋁條放入NaOH溶液中 | 立刻產生大量無色氣泡,鋁條逐漸變細,鋁條逐漸發熱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
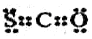
 ,可以表示35Cl-,也可以表示37Cl-
,可以表示35Cl-,也可以表示37Cl- 可以表示甲烷分子,也可以表示四氯化碳分子
可以表示甲烷分子,也可以表示四氯化碳分子
| A. | ①③⑥ | B. | ②③④⑥ | C. | ①②④⑥ | D. | 全部正確 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 ,則該分子中含有碳碳三鍵的數目為( )
,則該分子中含有碳碳三鍵的數目為( )| A. | 3 | B. | 2 | C. | 4 | D. | 1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com