
【題目】奈必洛爾是一種用于血管擴張的降血壓藥物,

已知:乙酸酐的結構簡式為![]() 。
。
請回答下列問題:
(1)B的分子式為______________,反應①的反應類型為________________
(2)C所含官能團的名稱為__________________________________________。
(3)反應⑤的化學方程式為_________________,該反應的反應類型是_________________。
(4)寫出滿足下列條件的E的同分異構體的結構簡式:___________、______________。
Ⅰ.苯環上只有三個取代基
Ⅱ.核磁共振氫譜圖中只有4組吸收峰
Ⅲ.1mol該物質與足量NaHCO3溶液反應生成2molCO2
(5)根據已有知識并結合相關信息,寫出以![]() 為原料制備
為原料制備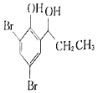 的合成路線流程圖(無機試劑任選)_____________。(合成路線流程圖示例如下:CH3CH2Br
的合成路線流程圖(無機試劑任選)_____________。(合成路線流程圖示例如下:CH3CH2Br![]() CH3CH2OHCH3COOCH2CH3)
CH3CH2OHCH3COOCH2CH3)
【答案】C8H7O2F 取代 氟原子、羰基、羥基 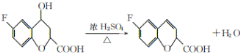 消去反應
消去反應 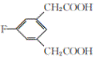
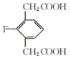

【解析】
A發生取代反應生成B,F與氫氣反應生成G,對比E、G的結構,則F結構簡式為:![]() ,反應⑤為醇羥基的消去反應;
,反應⑤為醇羥基的消去反應;
(5)由路線中B→C的轉化,![]() 在AlCl3的催化作用下轉化為
在AlCl3的催化作用下轉化為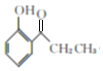 ,再與氫氣加成生成
,再與氫氣加成生成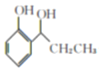 ,最后與溴發生取代反應生成
,最后與溴發生取代反應生成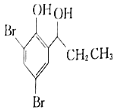 。
。
(1)B的結構簡式為 ,則分子式為C8H7O2F;反應①是
,則分子式為C8H7O2F;反應①是![]() 發生取代反應生成
發生取代反應生成 ;
;
(2)C的結構簡式為 ,所含官能團的名稱為氟原子、羰基、酚羥基;
,所含官能團的名稱為氟原子、羰基、酚羥基;
(3) F結構簡式為:![]() ,E發生消去反應生成F,則反應⑤的化學方程式為
,E發生消去反應生成F,則反應⑤的化學方程式為 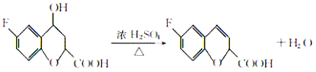 ,該反應的反應類型是消去反應;
,該反應的反應類型是消去反應;
(4) E的同分異構體符合下列條件:Ⅰ.苯環上只有三個取代基;Ⅱ.核磁共振氫譜圖中只有4組吸收峰,說明含有4種氫原子;Ⅲ.1mol該物質與足量NaHCO3溶液反應生成2molCO2,則說明含有2個羧基,符合條件的E的同分異構體結構簡式為: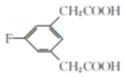 、
、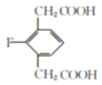 ;
;
(5) 由路線中B→C的轉化,![]() 在AlCl3的催化作用下轉化為
在AlCl3的催化作用下轉化為 ,再與氫氣加成生成
,再與氫氣加成生成 ,最后與溴發生取代反應生成
,最后與溴發生取代反應生成 ,合成路線流程圖為:
,合成路線流程圖為: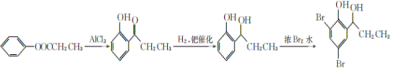 。
。


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:
【題目】現有室溫下四種溶液,有關敘述不正確的是( )
編號 | ① | ② | ③ | ④ |
pH | 10 | 10 | 4 | 4 |
溶液 | 氨水 | 氫氧化鈉溶液 | 醋酸溶液 | 鹽酸 |
A.相同體積③、④溶液分別與NaOH完全反應,消耗NaOH物質的量:③>④
B.分別加水稀釋10倍,四種溶液的pH:①>②>④>③
C.①、④兩溶液等體積混合,所得溶液為堿性
D.VaL④溶液與VbL②溶液混合(近似認為混合溶液體積=Va+Vb),若混合后溶液pH=5,則Va︰Vb=9︰11
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.紅磷P(s)和Cl2(g)發生反應生成PCl3和PCl5,反應過程和能量關系如圖所示(圖中的ΔH表示生成1mol產物的數據),根據下圖回答下列問題:

(1)PCl5分解生成PCl3和Cl2的熱化學方程式____________________;上述分解反應是一個可逆反應,溫度T1時,在密閉容器中加入0.8molPCl5,反應達到平衡時還剩余0.6molPCl5,其分解率α1等于________;若反應溫度由T1升高到T2,平衡時PCl5的分解率α2,α2________α1(填“大于”、“小于”或“等于”)。
(2)工業上制備PCl5通常分兩步進行,先將P和Cl2反應生成中間產物PCl3,然后降溫,再和Cl2反應生成PCl5。原因是_________________________________________________。
(3)P和Cl2分兩步反應生成1molPCl5的ΔH3=____________。
Ⅱ.某學生做濃度對化學反應速率的影響的實驗時,將2支試管編號為①②,并按下表中物質的量進行實驗,記錄的時間數據是:16s、28s。請將2個數據填入下表的適當位置,并寫出實驗結論。
試管編號 | 加入3%Na2S2O3 | 加H2O | 加稀鹽酸(1∶5) | 出現渾濁時間 |
① | 3mL | 3mL | 5滴 | a._____s |
② | 4mL | 2mL | 5滴 | b._____s |
(1)將對應①②的時間分別寫出:a.____________,b.____________。
(2)實驗結論____________________________________。
(3)寫出反應的化學方程式_______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關有機化合物的用途及性質的說法正確的是
A.乙烯使酸性KMnO4溶液或溴的CCl4溶液褪色的原理相同
B.苯與液溴在催化劑作用下生成溴苯發生了加成反應
C.淀粉、蛋白質等營養物質在人體內水解生成水和CO2等
D.用K2Cr2O7檢驗司機是否酒駕利用了乙醇的揮發性和還原性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家積極探索新技術對CO2進行綜合利用, CO2可用來合成低碳烴。
CO2(g) +4H2(g) ![]() CH4(g) + 2H2O(g) ΔH= a kJ/mol
CH4(g) + 2H2O(g) ΔH= a kJ/mol
(1)已知:①4H2(g)+ 2O2(g)=4H2O(g) △H=-967.2kJ/mol.
②CH4(g) + 2O2(g) =CO2(g) + 2H2O(g) ΔH=-802.0 kJ/mol.
請回答:①②這兩個反應在熱力學上趨勢均很大,其原因是__________________; a=____________kJ/mol。
(2)在體積為1L的密閉剛性容器中,充入4mol H2和1mol CO2,測得溫度對CO2的平衡轉化率和催化劑催化效率的影響如圖1所示。
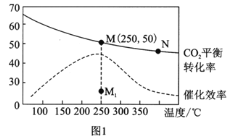
①已知M點總壓為1MPa,該反應在此溫度下的平衡常數Kp=______MPa-2。(Kp是用平衡分壓代替平衡濃度表示的化學平衡常數,氣體分壓=氣體總壓×體積分數。)
②欲增加二氧化碳的平衡轉化率,可采取的措施有__________。
A.通入惰性氣體 B.提高溫度
C.增加二氧化碳濃度 D.增加氫氣濃度
③下列說法正確的是_________。
A.平衡常數大小:KN>KM
B.其他條件不變,若不使用催化劑,則250℃ 時CO2的平衡轉化率可能位于點M1
C.圖1中M點時,甲烷的體積分數為12.5%
D.當壓強或n( H2)/n(CO2)不變時均可證明化學反應已達到平衡狀態
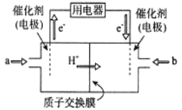
(3)新型高效的甲烷燃料電池工作時總反應式:CH4+2O2=CO2+2H2O。
①該電池的負極是___________(填a或b),②負極電極反應式為___________;
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下進行反應:COCl2(g)![]() Cl2 (g)+CO(g)。向2.0 L恒容密閉容器中充入1.0 mol COCl2 (g),經過一段時間后達到平衡。反應過程中測得的有關數據見下表:
Cl2 (g)+CO(g)。向2.0 L恒容密閉容器中充入1.0 mol COCl2 (g),經過一段時間后達到平衡。反應過程中測得的有關數據見下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2) /mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列說法正確的是 ( )
A.保持其他條件不變,升高溫度,平衡時c(Cl2) = 0.22 mol·L-1,則反應的 △H < 0
B.若在2 L恒容絕熱(與外界沒有熱量變換)密閉容器進行該反應,化學平衡常數不變
C.保持其他條件不變,起始向容器中充入1.2 mol COCl2、0.60 mol Cl2和0.6 mol CO,反應達到平衡前的速率:v (正) > v (逆)
D.保持其他條件不變,起始向容器中充入1.0 mol Cl2和0.8 mol CO,達到平衡時,Cl2的轉化率小于60%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)只用水就能鑒別的一組物質是______
a.苯、乙酸、四氯化碳 b.乙醇、乙醛、乙酸
c.乙醛、乙二醇、硝基苯 d.苯酚、乙醇、甘油
(2)現有化合物:甲: 乙:
乙: 丙:
丙:
①請寫出丙中含氧官能團的名稱:____。
②請判別上述哪些化合物互為同分異構體:____(填代號)。
(3)A和B兩種物質的分子式都是C7H8O芳香族化合物,它們都能跟金屬Na反應放出H2;A不溶于NaOH溶液而B能溶于NaOH溶液,B能使FeCl3溶液顯紫色,A不能;B苯環上的一溴代物有兩種結構。則A和B的名稱及結構簡式為:A_____,B_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】納米級Fe3O4呈黑色,因其有磁性且粒度小而在磁記錄材料、生物功能材料等諸多領域有重要應用,探究其制備和用途意義重大。
(1)還原-沉淀法:①用還原劑Na2SO3將一定量Fe3+可溶鹽溶液中的![]() Fe3+還原,使Fe2+和Fe3+的物質的量比為1 : 2。②然后在①所得體系中加入氨水,鐵元素完全沉淀形成納米Fe3O4。寫出②過程的離子方程式:__________。
Fe3+還原,使Fe2+和Fe3+的物質的量比為1 : 2。②然后在①所得體系中加入氨水,鐵元素完全沉淀形成納米Fe3O4。寫出②過程的離子方程式:__________。
(2)電化學法也可制備納米級Fe3O4,用面積為4 cm2的不銹鋼小球(不含鎳、鉻)為工作電極,鉑絲作陰極,用Na2SO4溶液作為電解液,電解液的pH維持在10左右,電流50 mA。生成Fe3O4的電極反應為______。
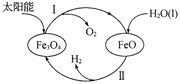
(3)已知:H2O(1) === H2(g)+![]() O2(g) △H =+285.5 kJ·mol-l,以太陽能為熱源分解Fe3O4,經由熱化學鐵氧化合物循環分解水制H2的過程如下,完善以下過程I的熱化學方程式。過程I:__________。過程Ⅱ:3FeO(s)+H2O(l) === H2(g)+Fe3O4(s) △H =+128.9 kJ·mol-1
O2(g) △H =+285.5 kJ·mol-l,以太陽能為熱源分解Fe3O4,經由熱化學鐵氧化合物循環分解水制H2的過程如下,完善以下過程I的熱化學方程式。過程I:__________。過程Ⅱ:3FeO(s)+H2O(l) === H2(g)+Fe3O4(s) △H =+128.9 kJ·mol-1
(4)磁鐵礦(Fe3O4)常作冶鐵的原料,主要反應為Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2 (g),該反應的△H < 0,T℃時,在1 L恒容密閉容器中,加入Fe3O4、CO各0.5 mol,10 min后反應達到平衡時,容器中CO2的濃度是0.4 mol·L-1。
3Fe(s)+4CO2 (g),該反應的△H < 0,T℃時,在1 L恒容密閉容器中,加入Fe3O4、CO各0.5 mol,10 min后反應達到平衡時,容器中CO2的濃度是0.4 mol·L-1。
①T℃時,10 min內用Fe3O4表示的平均反應速率為___g·min-1。
②T℃時,該反應的平衡常數為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學家創造性地構建了硅化物晶格限域的單鐵中心催化劑,成功地實現了甲烷在無氧條件下選擇活化,一步高效生產乙烯、芳烴和氫氣等化學品。請回答下列問題:
(1)基態鐵原子的價層電子軌道表達式為______。
(2)硅、碳位于同一主族,用“![]() ”“
”“![]() ”或“
”或“![]() ”填空:
”填空:
性質 | 原子半徑 | 第一電離能 | 熔點 | 鍵能 |
項目 |
|
|
|
|
(3)CN-能與Fe3+形成配合物,與CN-互為等電子體的分子有______ (任寫一種);1 mol[Fe(CN)6 ]3-中含______molσ鍵。
(4)已知:反應![]() ,碳原子的雜化類型轉化過程為______;
,碳原子的雜化類型轉化過程為______;
從共價鍵重疊方式看,![]() 分子中
分子中![]() 鍵類型為;
鍵類型為;![]() 的鍵角比
的鍵角比![]() 的鍵角______
的鍵角______![]() 填“大”或“小”
填“大”或“小”![]() 。
。
(5)晶體有兩種晶胞,如圖1、圖2所示。

圖1中晶胞中鐵的配位數為______;圖2中鐵晶胞堆積方式為______。
(6)碳化硅晶胞如圖3所示,已知碳化硅晶體的密度為dgcm-3,NA表示阿伏加德羅常數的值,則碳化硅中硅碳鍵的鍵長為______ pm。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com