
分析 (1)取原溶液少量于試管中,向試管中不斷加入氫氧化鈉溶液至過量,有白色沉淀生成而后又完全消失,說明原溶液中一定含有Al3+,一定不含Mg2+;
(2)取實驗①后的溶液于另一試管中,加熱,用濕潤的紅色石蕊試紙置于試管口,結果試紙變藍,應生成氨氣,說明含有NH4+;
(3)取原溶液加入少量鹽酸使溶液酸化,再加入氯化鋇溶液,產生白色沉淀,說明含有SO42-;
(4)取實驗③的溶液加入少量,加入硝酸銀溶液,產生白色沉淀,說明生成AgCl,但不能說明原溶液含有Cl-,因實驗(3)加入氯化鋇.
解答 解:(1)取原溶液少量于試管中,向試管中不斷加入氫氧化鈉溶液至過量,有白色沉淀生成而后又完全消失,說明原溶液中一定含有Al3+,故答案為:Al3+;
(2)取實驗①后的溶液于另一試管中,加熱,用濕潤的紅色石蕊試紙置于試管口,結果試紙變藍,應生成氨氣,說明含有NH4+,故答案為:NH4+;
(3)取原溶液加入少量鹽酸使溶液酸化,再加入氯化鋇溶液,產生白色沉淀,說明含有SO42-,故答案為:SO42-;
(4)取實驗③的溶液加入少量,加入硝酸銀溶液,產生白色沉淀,說明生成AgCl,但不能說明原溶液含有Cl-,因實驗(3)加入氯化鋇,若要檢測Cl-離子是否存在,正確的操作是取原溶液少量于試管中,用硝酸酸化,再滴加硝酸銀溶液,若有白色沉淀,證明氯離子存在,否則不含氯離子,
故答案為:否;取原溶液少量于試管中,用硝酸酸化,再滴加硝酸銀溶液,若有白色沉淀,證明氯離子存在,否則不含氯離子.
點評 本題考查物質的檢驗及鑒別,為高頻考點,把握常見離子之間的反應、離子檢驗等為推斷的關鍵,側重分析與推斷能力的綜合考查,題目難度不大.


 課課練江蘇系列答案
課課練江蘇系列答案 名牌中學課時作業系列答案
名牌中學課時作業系列答案 明天教育課時特訓系列答案
明天教育課時特訓系列答案 浙江新課程三維目標測評課時特訓系列答案
浙江新課程三維目標測評課時特訓系列答案科目:高中化學 來源: 題型:選擇題
| A. | 正極為Cu,負極為Fe,電解質溶液為FeCl3溶液 | |
| B. | 正極為C,負極為Fe,電解質溶液為FeSO4溶液 | |
| C. | 正極為Fe,負極為Zn,電解質溶液為Fe2(SO4)3溶液 | |
| D. | 正極為Ag,負極為Cu,電解質溶液為CuSO4溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗編號 | H2C2O4溶液 | 酸性KMnO4溶液 | 溫度 | ||
| 濃度(mol/L) | 體積(mL) | 濃度(mol/L) | 體積 (mL) | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用澄清石灰水可區別Na2CO3和NaHCO3粉末 | |
| B. |  用如圖裝置進行濃硝酸與銅的反應制取并收集NO2 用如圖裝置進行濃硝酸與銅的反應制取并收集NO2 | |
| C. | 檢驗未知溶液是否含SO42ˉ可先加氯化鋇,再加稀鹽酸 | |
| D. | 除去粗鹽中的Ca2+、Mg2+、SO42-,可依次加入H2O、NaOH、BaCl2、Na2CO3,過濾再加入HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
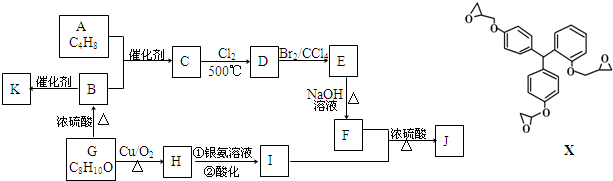
 .
.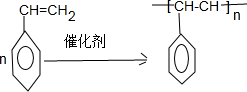 ;F+I→J
;F+I→J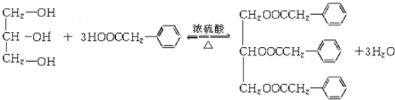 .
. (其中三種).
(其中三種).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
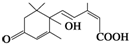 官能團的名稱:碳碳雙鍵、羰基、羥基、羧基.
官能團的名稱:碳碳雙鍵、羰基、羥基、羧基. 2,3-二甲基戊烷
2,3-二甲基戊烷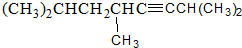 2,5,7-三甲基-3-辛炔
2,5,7-三甲基-3-辛炔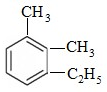
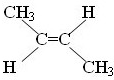 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com