
| A. | 等物質的量濃度的FeBr2和CuCl2混合溶液用惰性電極電解最初發生:Cu 2++2Br- $\frac{\underline{\;電解\;}}{\;}$Cu+Br2 | |
| B. | Na2S溶液水解:S2-+2H2O?H2S+2OH- | |
| C. | Fe(NO3)3的酸性溶液中通入足量硫化氫:2Fe3++H2S=2Fe2++S↓+2H+ | |
| D. | H218O中投入Na2O2:2H218O+2Na2O2=4Na++4OH-+18O2↑ |
分析 A.陰極上陽離子氧化性強的銅離子先得到電子,陰極上還原性強的溴離子失去電子;
B.硫離子水解分步進行,以第一步為主;
C.硫化氫足量,酸性溶液中,氧化性HNO3>Fe3+,則Fe(NO3)3完全反應;
D.Na2O2為氧化劑,也為還原劑.
解答 解:A.等物質的量濃度的FeBr2和CuCl2混合溶液用惰性電極電解最初發生的離子反應為Cu2++2Br- $\frac{\underline{\;電解\;}}{\;}$Cu+Br2,故A正確;
B.Na2S溶液水解的離子反應為S2-+H2O?HS-+OH-,故B錯誤;
C.因硫化氫足量,則Fe(NO3)3完全反應,離子反應為Fe3++3NO3-+2H++5H2S═Fe2++3NO↑+6H2O+5S↓,故C錯誤;
D.H218O中投入Na2O2:的離子反應為2H218O+2Na2O2=4Na++2OH-+218OH-+O2↑,故D錯誤;
故選A.
點評 本題考查離子反應方程式書寫的正誤判斷,為高頻考點,把握發生的反應及離子反應的書寫方法為解答的關鍵,側重電解、水解反應、氧化還原反應的離子反應考查,注意離子反應中保留化學式的物質及電子、電荷守恒分析,綜合性較強,題目難度不大.


科目:高中化學 來源: 題型:選擇題
 噴泉是一種常見的自然現象,其產生的原因是存在壓強差,如圖所示裝置是常見的噴泉實驗裝置.在圓底燒瓶中分別收集干燥純凈的氣體,燒杯和膠頭滴管中分別盛放同一種液體.當擠入膠頭滴管中液體時,下列實驗不能出現噴泉現象的是( )
噴泉是一種常見的自然現象,其產生的原因是存在壓強差,如圖所示裝置是常見的噴泉實驗裝置.在圓底燒瓶中分別收集干燥純凈的氣體,燒杯和膠頭滴管中分別盛放同一種液體.當擠入膠頭滴管中液體時,下列實驗不能出現噴泉現象的是( )| 氣 體 | 液 體 | 氣 體 | 液 體 | ||
| A | HCl | 蒸餾水 | B | SO2 | 濃燒堿液 |
| C | NO | 濃燒堿液 | D | NH3 | 蒸餾水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 最外層只有1個電子的元素一定是金屬元素 | |
| B. | 最外層只有2個電子的元素一定是金屬元素 | |
| C. | 原子核外各層電子數相等的元素不一定是金屬元素 | |
| D. | 核電荷數為17的元素的原子易獲得1個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
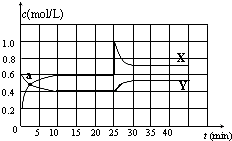 已知NO2和N2O4可以相互轉化:N2O4(g)?2NO2(g)△H<0.在恒溫條件下將一定量NO2和N2O4的混合氣體通入一容積為2L的密閉容器中,反應物濃度隨時間變化關系如圖.下列說法不正確的是( )
已知NO2和N2O4可以相互轉化:N2O4(g)?2NO2(g)△H<0.在恒溫條件下將一定量NO2和N2O4的混合氣體通入一容積為2L的密閉容器中,反應物濃度隨時間變化關系如圖.下列說法不正確的是( )| A. | 圖中的兩條曲線,X是表示NO2濃度隨時間的變化曲線 | |
| B. | a點時v(N2O4)=v(NO2) | |
| C. | 25min時改變了影響速率的一個因素,使得NO2轉變為N2O4,該改變是將密閉容器的體積縮小,增大壓強 | |
| D. | 前10min內用v(N2O4)表示的化學反應速率為0.02 mol/(L•min) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2(g)+0.5O2(g)?SO3(g)△H=-213kJ•mol-1 說明25℃,101kPa下,lmolSO2與0.5mol氧氣放入密閉容器中生成SO3時放出213 kJ熱量 | |
| B. | 若反應物總能量高于生成物總能量,反應放熱,△H<0 | |
| C. | 化學反應必然伴隨能量變化 | |
| D. | 酸和堿的中和反應都是放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
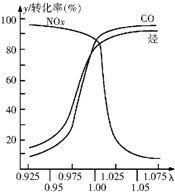 隨著經濟的發展和生活水平的提高,近年來我省汽車擁有量呈較快增長趨勢.
隨著經濟的發展和生活水平的提高,近年來我省汽車擁有量呈較快增長趨勢.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| X | Y | ||
| Z | W | Q |
 .
. .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com