
 .
. 、
、 、
、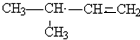 (任意一種);(寫出其中的一種)
(任意一種);(寫出其中的一種)分析 (1)令烴的組成為CxHy,相同物質的量的烴,耗氧量取決于(x+$\frac{y}{4}$),(x+$\frac{y}{4}$),值越大耗氧量越大;
乙烷、丙烯、丁炔的分子式分別為C2H6、C3H6、C4H6,分子中含有的H原子數目相同,根據氫元素守恒可知,物質的量相同生成水的質量相同;
1mol某不飽和烴可以和1molCl2發生加成反應,生成2,3-二氯-2-甲基戊烷,根據加成反應的原理,采取倒推法還原C=C雙鍵,從分子中減掉氯原子形成C=C雙鍵,可得不飽和烴的結構,再根據系統命名法進行命名;
(2)①烴燃燒生成二氧化碳和水,由0.2mol烴燃燒生成B、C即二氧化碳和水各1mol,根據C、H守恒判斷分子式;
②若烴A不能使溴水褪色,但在一定條件下,能與Cl2發生取代反應,其一氯代物只有一種,說明烴中不含碳碳雙鍵,應為環烷烴,即環戊烷;
③烴A能使溴水褪色,在催化劑作用下,與H2加成,其加成產物經測定分子中含有3個甲基,說明烴中含有C=C,其中含有3個甲基的有3種,以此確定烯烴;
(3)甲苯可被酸性高錳酸鉀氧化,乙醇易溶于水,溴可與氫氧化鈉溶液反應.
解答 解:(1)乙烷分子式為C2H6,其(x+$\frac{y}{4}$)=2+$\frac{6}{4}$=3.5,丙烯的分子式為C3H6,其(x+$\frac{y}{4}$)=3+$\frac{6}{4}$=4.5,丁炔的分子式為C4H6,其(x+$\frac{y}{4}$)=4+$\frac{6}{4}$=5.5,故相同物質的量的烴,丁炔的耗氧量最多;
乙烷、丙烯、的分子式分別為C2H6、C3H6、C4H6,分子中含有的H原子數目相同,根據氫元素守恒可知,物質的量相同生成水的質量相同;
1mol某不飽和烴可以和1molCl2發生加成反應,生成2,3-二氯-2-甲基戊烷,根據加成反應的原理,采取倒推法還原C=C雙鍵,從分子中減掉氯原子形成C=C雙鍵,可得不飽和烴的結構為(CH3)2C=CH-CH2-CH3,根據系統命名法命名為2-甲基-2-戊烯.
故答案為:丁炔; 水;C(CH3)2=CHCH2CH3;2-甲基-2-戊烯;
(2)①某烴A 0.2mol 在氧氣中完全燃燒后,生成B、C即CO2和H2O各1mol,則分子中含有N(C)=5,n(H)=10,分子式為C5H10,故答案為:C5H10;
②若烴A不能使溴水褪色,但在一定條件下,能與Cl2發生取代反應,其一氯代物只有一種,說明烴中不含碳碳雙鍵,應為環烷烴,即環戊烷,結構簡式為 ,故答案為:
,故答案為: ;
;
③烴A能使溴水褪色,在催化劑作用下,與H2加成,其加成產物經測定分子中含有3個甲基,說明烴中含有C=C,其中含有 3個甲基的有3種,烴A可能有的結構簡式為 、
、 、
、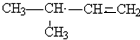 ,
,
故答案為: 、
、 、
、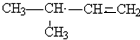 ;
;
(3)甲苯可被酸性高錳酸鉀氧化,生成的苯甲酸可溶于水,乙醇易溶于水,可加水分離,溴可與氫氧化鈉溶液反應,然后分層分離,
故答案為:酸性KMnO4溶液; 水; NaOH溶液.
點評 本題考查有機物的推斷,側重于有機物的結構和性質的考查,為高考常見題型,題目難度中等,本題側重于同分異構體的判斷、有機反應的計算以及鑒別,注意根據物質的性質判斷可能具有的結構.


 培優好卷單元加期末卷系列答案
培優好卷單元加期末卷系列答案 一線名師權威作業本系列答案
一線名師權威作業本系列答案科目:高中化學 來源: 題型:選擇題
| A. | ②④①③ | B. | ②①④③ | C. | ①②③④ | D. | ①②④③ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯與硝酸在加熱時發生取代反應,甲苯與硝酸在常溫下就能發生取代反應 | |
| B. | 乙醇、苯酚都有羥基,但是電離常數不同 | |
| C. | 苯酚無需催化劑即能與溴水發生取代反應 | |
| D. | 1 mol甲苯能與3 mol H2發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 甲烷分子中的4個氫原子都可以被取代,若甲烷分子中的4個氫原子都被苯基取代,可以得到的分子如圖,對該分子的描述,不正確的是( )
甲烷分子中的4個氫原子都可以被取代,若甲烷分子中的4個氫原子都被苯基取代,可以得到的分子如圖,對該分子的描述,不正確的是( )| A. | 分子式為C25H20 | B. | 所有的碳原子可能都在同一平面上 | ||
| C. | 所有原子一定在同一平面上 | D. | 此物質屬于芳香烴類物質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol H2O和D2O組成的混合物中含有中子數是NA | |
| B. | 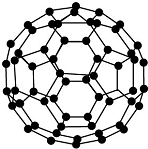 28 g N60(分子結構如圖所示)中含有的N-N鍵數目為1.5NA | |
| C. | 0℃、1.01×105 Pa時,11.2 L氧氣中所含的原子數約為NA | |
| D. | 常溫下,將5.6 g鐵投入足量的稀硫酸中,充分反應,轉移電子數為0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
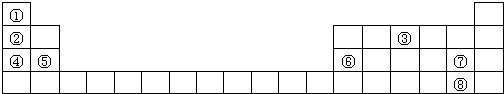
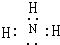 ,實驗室制取該氫化物的化學方程式為2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
,實驗室制取該氫化物的化學方程式為2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O. .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com