
| A. | H2S>I2>Fe3+>Cl2 | B. | Cl2>Fe3+>I2>H2S | ||
| C. | Fe3+>Cl2>H2S>I2. | D. | Cl2>I2>Fe3+>H2S |
分析 同一化學反應中,氧化劑的氧化性大于氧化產物的氧化性,根據元素化合價的變化判斷氧化劑和氧化產物,據此分析解答.
解答 解:(1)Cl2+2KI=2KCl+I2 反應中Cl2做氧化劑,氧化KI得到氧化產物I2,氧化性:Cl2>I2;
(2)2FeCl2+Cl2=2FeCl3反應中Cl2做氧化劑,氧化FeCl2得到氧化產物FeCl3,氧化性:Cl2>FeCl3;
(3)2FeCl3+2HI=2FeCl2+2HCl+I2 反應中FeCl3做氧化劑,氧化HI得到氧化產物I2,氧化性:FeCl3>I2;
(4)H2S+I2=2HI+S反應中I2做氧化劑,氧化H2S得到氧化產物S,氧化性:I2>S;
則氧化性順序為:Cl2>FeCl3>I2>S,
故選B.
點評 本題考查了根據方程式來比較氧化性和還原性,解題的關鍵是根據化合價找出氧化劑、還原劑、氧化產物和還原產物,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
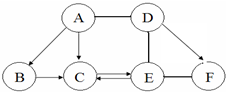 如圖 A、B、C、D、E、F為初中化學常見的六種含氧化合物,A、B、C 均由兩種元素組成,在常溫下狀態各不相同,其中A為紅色粉末,D、E、F 均由三種元素組成,且物質類別各不相同.“→”表示物質間的轉化關系,“-”表示兩種物質能相互反應(部分反應物、生成物及反應條件未標出).回答下列問題:
如圖 A、B、C、D、E、F為初中化學常見的六種含氧化合物,A、B、C 均由兩種元素組成,在常溫下狀態各不相同,其中A為紅色粉末,D、E、F 均由三種元素組成,且物質類別各不相同.“→”表示物質間的轉化關系,“-”表示兩種物質能相互反應(部分反應物、生成物及反應條件未標出).回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
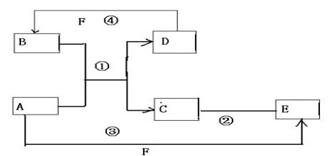
 反應?①的化學方程式2NH3+3Cl2=N2+6HCl
反應?①的化學方程式2NH3+3Cl2=N2+6HCl查看答案和解析>>
科目:高中化學 來源: 題型:解答題
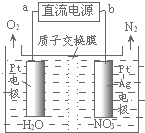 發生在天津港“8•12”特大火災爆炸事故,再一次引發了人們對環境問題的關注.
發生在天津港“8•12”特大火災爆炸事故,再一次引發了人們對環境問題的關注.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 14C原子的結構示意圖: | |
| B. | H2O2的電子式: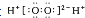 | |
| C. | NH4C的電子式: | |
| D. | 原子核內有10個中子的氧原子${\;}_{8}^{16}$O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
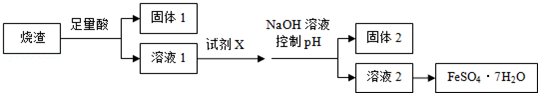
| A. | 溶解燒渣選用足量硫酸,試劑X選用鐵粉 | |
| B. | 固體1中一定含有SiO2,控制pH是為了使Al3+轉化為Al3,進入固體2 | |
| C. | 從溶液2得到FeSO4•7H2O產品的過程中,須控制條件防止其氧化和分解 | |
| D. | 若改變方案,在溶液1中直接加NaOH至過量,得到的沉淀用硫酸溶解,其溶液經結晶分離也可得到FeSO4•7H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com