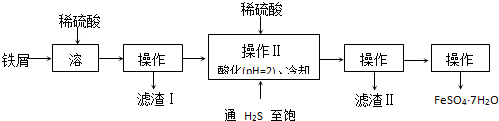
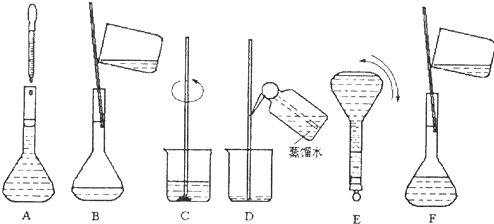
(1)下列根據實驗事實得出的結論,正確的有
(填序號)
①試液
顏色無變化
溶液變為血紅色
結論:試液中含有Fe
2+②試液
白色沉淀
沉淀不溶解
結論:試液中含有SO
42-③Ba(OH)
2溶液
溶液的導電能力先減弱后增強
結論:Ba(OH)
2和H
2SO
4之間的反應是離子反應
④稀硫酸
產生少量氣泡
產生大量氣泡,
結論:CuSO
4是鋅與稀硫酸反應的催化劑
(2)現有三位同學分別利用濃鹽酸、MnO
2共熱制Cl
2,并用Cl
2和Ca(OH)
2反應制取少量漂白粉,設計了三套實驗裝置:
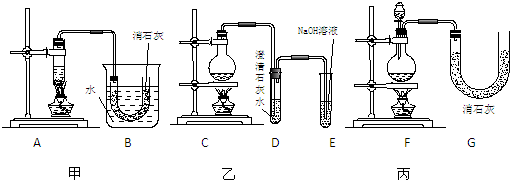
已知:溫度稍高即發生如下副反應:6Cl
2+6Ca(OH)
2=Ca(ClO
3)
2+5CaCl
2+6H
2O
1.請寫出制備氯氣時發生反應的化學反應方程式,并用單線橋法表示出電子轉移.
2.三位同學所設計的裝置都有優點和缺點,請從你的角度分析甲同學裝置的優缺點.優點:
.
缺點:
.請從上述裝置的A-G的組成中選取合理的部分組裝一套較完善的實驗裝置,裝置各部分的連接順序(按氣流從左到右的方向)是
.
3.近幾年歐美發達國家使用了一種更安全、高效的殺菌消毒物質二氧化氯.它對水中的重金屬離子和氰化物都有很高的去除效果.二氧化氯可以將氰化物轉化成兩種空氣成分氣體.請寫出過程中所發生反應的離子方程式:
.


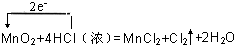 ,故答案為:
,故答案為: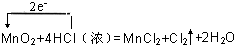 ;
;

 各地期末復習特訓卷系列答案
各地期末復習特訓卷系列答案 小博士期末闖關100分系列答案
小博士期末闖關100分系列答案 如圖是某學生設計的制取和收集某些氣體的實驗裝置(可加熱).
如圖是某學生設計的制取和收集某些氣體的實驗裝置(可加熱).