
【題目】為驗證鹵素單質氧化性的相對強弱,某學習小組用下圖所示裝置進行實驗(夾持儀器已略去,氣密性已檢驗)。實驗過程:
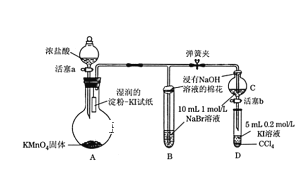
Ⅰ. 打開彈簧夾,打開活塞a,滴加濃鹽酸。
Ⅱ. 當B和C中的溶液都變為黃色時,夾緊彈簧夾。
Ⅲ. 當B中溶液由黃色變為棕紅色時,關閉活塞a。
Ⅳ.……
回答問題:
(1)A中產生黃綠色氣體,其電子式是_________。實驗室在加熱條件下制取該氣體的離子方程式為____________。
(2)驗證氯氣的氧化性強于碘單質的實驗現象是____________。
(3)C中溶液發生反應的離子方程式是_______________。
(4)過程Ⅲ實驗的目的:甲同學認為試管B的作用就是吸收尾氣,防止多余Cl2污染空氣,因此B中盛裝的最佳試劑應該為__________________________
乙同學經分析認為,B中溶液由黃色變為棕紅色,發生反應為Cl2+2NaBr=2NaCl+Br2,以此說明C中________,從而得出D中氧化I-的氧化劑必為_______,因此B裝置是必不可少的。
(5)過程Ⅳ為:打開活塞b,將少量C中溶液滴入D中,關閉活塞b,取下試管D震蕩,靜置,觀察到的現象為______________,發生反應的離子方程式為_____________________。
(6)氯、溴、碘單質的氧化性逐漸減弱的本質原因:同主族元素從上到下_________,得電子能力逐漸減弱。
【答案】![]() MnO2+4H++2Cl-
MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O 淀粉KI試紙變藍 Cl2+2Br-=Br2+2Cl- 氫氧化鈉溶液 無Cl2,排除Cl2對溴置換碘實驗的干擾 Br2 CCl4層溶液變為紫紅色 Br2+2I-=I2+2Br - 原子半徑逐漸增大
Mn2++Cl2↑+2H2O 淀粉KI試紙變藍 Cl2+2Br-=Br2+2Cl- 氫氧化鈉溶液 無Cl2,排除Cl2對溴置換碘實驗的干擾 Br2 CCl4層溶液變為紫紅色 Br2+2I-=I2+2Br - 原子半徑逐漸增大
【解析】
裝置A中高錳酸鉀固體與濃鹽酸反應生成氯化錳、氯化鉀、氯氣和水,反應生成的氯氣使濕潤的淀粉KI試紙變藍;裝置B、C中氯氣與溴化鈉溶液發生置換反應生成氯化鈉和單質溴,浸有氫氧化鈉溶液棉花吸收有毒的氯氣,防止污染環境;裝置D中反應生成的單質溴與碘化鈉和四氯化碳混合溶液發生置換反應生成氯化鈉和單質碘,震蕩,靜置,溶液分層,下層溶液變為紫紅色,該實驗說明氯、溴、碘單質的氧化性逐漸減弱。
(1)A中產生黃綠色氣體為氯氣,氯氣是雙原子分子,電子式為![]() ;實驗室用二氧化錳與濃鹽酸共熱反應制備氯氣,反應的離子方程式為MnO2+4H++2Cl-
;實驗室用二氧化錳與濃鹽酸共熱反應制備氯氣,反應的離子方程式為MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O,故答案為:
Mn2++Cl2↑+2H2O,故答案為:![]() ;MnO2+4H++2Cl-
;MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)裝置A中反應生成的氯氣使濕潤的淀粉KI試紙變藍,說明氯氣與碘化鉀發生置換反應生成單質碘和氯化鉀,由氧化劑的氧化性大于氧化產物的氧化性可知Cl2的氧化性大于I2的氧化性,故答案為:濕潤的淀粉KI試紙變藍;
(3)裝置C中氯氣與溴化鈉溶液發生置換反應生成氯化鈉和單質溴,反應的離子方程式為Cl2+2Br-=Br2+2Cl-,故答案為:Cl2+2Br-=Br2+2Cl-;
(4)氯氣能與氫氧化鈉溶液反應生成氯化鈉、次氯酸鈉和水,若試管B的作用就是吸收氯氣,防止多余Cl2污染空氣,則最佳試劑為氫氧化鈉溶液;為驗證溴的氧化性強于碘,實驗時應避免氯氣的干擾,當B中溶液由黃色變為棕紅色時,說明有大量的溴生成,關閉活塞a,則C中無Cl2,排除了Cl2對溴置換碘實驗的干擾;由此可知裝置D中反應生成的單質溴做氧化劑,與碘化鈉和四氯化碳混合溶液發生置換反應生成氯化鈉和單質碘,故答案為:氫氧化鈉溶液;無Cl2,排除Cl2對溴置換碘實驗的干擾;Br2;
(5)裝置D中反應生成的單質溴與碘化鈉和四氯化碳混合溶液發生置換反應生成氯化鈉和單質碘,震蕩,靜置,溶液分層,下層溶液變為紫紅色,反應的離子方程式為Br2+2I-=I2+2Br -,故答案為:CCl4層溶液變為紫紅色;Br2+2I-=I2+2Br -;
(6)因同一主族元素,從上到下,電子層數依次增多,原子半徑逐漸增大,元素的金屬性逐漸增強,得電子能力逐漸減弱,故答案為:原子半徑逐漸增大。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】A是石油裂解氣的主要產物之一,其產量是衡量一個國家石油化工發展水平的標志。下列是有機物A~G之間的轉化關系:

請回答下列問題:
(1)D中所含官能團的名稱是_____________。
(2)反應③的化學方程式是_________________________________。
(3)G是一種高分子化合物,可以用來制造農用薄膜材料等,其結構簡式是___________。
(4)在體育競技比賽中,當運動員肌肉挫傷或扭傷時,隨隊醫生立即對準其受傷部位噴射物質F(沸點12.27℃)進行應急處理。A制備F的化學方程式是_____________。
(5)B與D反應加入濃硫酸的作用是_________;為了得到較純的E,需除去E中含有的D,最好的處理方法是_____________(用序號填寫)。
a.蒸餾 b.用過量飽和碳酸鈉溶液洗滌后分液 c.水洗后分液 d.用過量氯化鈉溶液洗滌后分液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度時,在2 L容器中A、B兩種物質間的轉化反應中,A、B物質的量隨時間變化的曲線如圖所示,由圖中數據分析得:
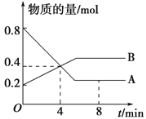
(1)該反應的化學方程式為___________________。
(2)反應開始至4 min時,A的平均反應速率為____________________________。
(3)4 min時,反應是否達到平衡狀態?________(填“是”或“否”),8 min時,v(正)________v(逆) (填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,在恒容密閉容器中,能表示反應X(g)+2Y(g) ![]() 2Z(g)一定達到化學平衡狀態的是( )
2Z(g)一定達到化學平衡狀態的是( )
①X、Y、Z的物質的量之比為1∶2∶2
②X、Y、Z的濃度不再發生變化
③容器中的壓強不再發生變化
④單位時間內生成n mol Z,同時生成2n mol Y
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化學 來源: 題型:
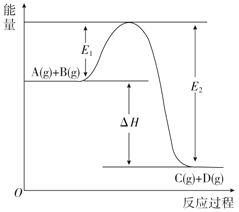
【題目】反應A(g)+B(g)═C(g)+D(g)過程中的能量變化如圖所示,回答下列問題.
(1)該反應是_____反應(填“吸熱”或“放熱”),
(2)E1表示____________,E2表示_____, △H=______,
(3)反應體系中加入催化劑對反應熱是否有影響?_______(填“有影響”“無影響”),
(4)在反應體系中加入催化劑,E1和E2的變化是:E1____,E2____(填“增大”“減小”或“不變”).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(題文)50 mL 0.50 mol·L-1的鹽酸與50 mL 0.55 mol·L-1NaOH溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱,完成下列問題: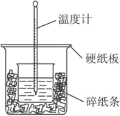
(1)從實驗裝置上看,圖中尚缺少的一種玻璃用品是_____________。請指出裝置中的另外錯誤是 ________________________
(2)燒杯間填滿碎紙條的作用是___________。
(3)大燒杯上如不蓋硬紙板,求得的中和熱值___________(填“偏大”“偏小”“無影響”)。
(4)實驗中改用60 mL 0.50mol·L-1的鹽酸跟60 mL 0.55mol·L-1NaOH溶液進行上述實驗相比,所放出的熱量___________(填“相等”“不相等”),所求中和熱___________(填“相等”“不相等”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素X、Y、Z、W在元素周期表中的相對位置如下圖所示,其中W原子的質子數是其最外層電子數的三倍,下列說法不正確的是( )

A. 原子半徑:W>Z>Y>X
B. 最高價氧化物對應水化物的酸性:X>W>Z
C. 最簡單氣態氫化物的熱穩定性:Y>X>W>Z
D. 元素X、Z、W的最高化合價分別與其主族序數相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組要完成中和熱的測定。
(1)實驗桌上備有大、小兩個燒杯、量筒、泡沫塑料、泡沫塑料板、膠頭滴管、0.5 mol·L-1鹽酸、0.55 mol·L-1NaOH溶液,實驗尚缺少的玻璃用品是______、_______________。他們記錄的實驗數據如下:
實驗用品 | 溶液溫度 | 中和熱 | |||
t1 | t2 | ΔH | |||
① | 50 mL0.55 mol·L-1NaOH溶液 | 50 mL0.5mol·L-1HCl溶液 | 20 ℃ | 23.3 ℃ | |
② | 50 mL0.55 mol·L-1NaOH溶液 | 50 mL0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.5 ℃ | |
已知:Q=cm(t2-t1),反應后溶液的比熱容c為4.18 kJ·℃-1·kg-1,各物質的密度均為1 g·cm-3。
(2)NaOH用量比HCl用量稍多的原因是_________________________________。
(3)根據實驗結果寫出NaOH溶液與HCl溶液反應的熱化學方程式: ___________________。
(4)若用KOH代替NaOH,對測定結果________(填“有”或 “無”)影響;若用醋酸代替HCl做實驗,對測定結果__________(填“有”或“無”)影響。
(5)兩溶液混合后,怎樣攪拌溶液_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應mA(s)+nB(g)![]() pC(g)△H<0,在一定溫度下,平衡時B的體積分數(B%)與壓強變化的關系如圖所示,下列敘述中一定正確的是( )
pC(g)△H<0,在一定溫度下,平衡時B的體積分數(B%)與壓強變化的關系如圖所示,下列敘述中一定正確的是( )
①m+n>p ②x點表示的正反應速率大于逆反應速率
③x點比y點時的反應速率慢 ④n>p
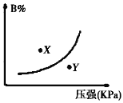
A. ①② B. ②④ C. ②③ D. ①③
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com