
【題目】A是石油裂解氣的主要產物之一,其產量是衡量一個國家石油化工發展水平的標志。下列是有機物A~G之間的轉化關系:

請回答下列問題:
(1)D中所含官能團的名稱是_____________。
(2)反應③的化學方程式是_________________________________。
(3)G是一種高分子化合物,可以用來制造農用薄膜材料等,其結構簡式是___________。
(4)在體育競技比賽中,當運動員肌肉挫傷或扭傷時,隨隊醫生立即對準其受傷部位噴射物質F(沸點12.27℃)進行應急處理。A制備F的化學方程式是_____________。
(5)B與D反應加入濃硫酸的作用是_________;為了得到較純的E,需除去E中含有的D,最好的處理方法是_____________(用序號填寫)。
a.蒸餾 b.用過量飽和碳酸鈉溶液洗滌后分液 c.水洗后分液 d.用過量氯化鈉溶液洗滌后分液
【答案】羧基 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O ![]() CH2=CH2+HCl
CH2=CH2+HCl ![]() CH3CH2Cl 催化劑和吸水劑 b
CH3CH2Cl 催化劑和吸水劑 b
【解析】
A是石油裂解氣的主要產物之一,它的產量用來衡量一個國家的石油化工發展水平,則A為C2H4;由轉化關系可知乙烯和氯化氫發生加成反應生成F,F為氯乙烷,乙烯和水發生加成反應生成B,則B是乙醇,乙醇和氧氣在銅作催化劑作用下催化反應生成C,則C是乙醛,B(乙醇)在高錳酸鉀作用下生成D,D是乙酸,乙醇和乙酸在濃硫酸作用下反應生成E,E為乙酸乙酯;G是一種高分子化合物,由A乙烯加聚而成,G為聚乙烯,據此分析解答。
(1)D為乙酸,含有的官能團為羧基,故答案為:羧基;
(2)反應③為乙醇和氧氣在銅作催化劑作用下反應生成C,反應的化學方程式為2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O,故答案為:2CH3CH2OH+O2
2CH3CHO+2H2O,故答案為:2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(3)由以上分析可知,G為聚乙烯,其結構簡式為![]() ,故答案為:
,故答案為:![]() ;
;
(4)F為A乙烯和氯化氫反應的產物,乙烯和氯化氫在一定條件下發生加成反應生成氯乙烷,反應的化學方程式為:CH2=CH2+HCl ![]() CH3CH2Cl,故答案為:CH2=CH2+HCl
CH3CH2Cl,故答案為:CH2=CH2+HCl ![]() CH3CH2Cl;
CH3CH2Cl;
(5)乙醇與乙酸發生酯化反應,反應中需要加入濃硫酸,濃硫酸的作用為催化劑和吸水劑;為了得到較純的乙酸乙酯,需除去乙酸乙酯中含有的乙酸,乙酸能夠與碳酸鈉反應,而乙酸乙酯在碳酸鈉溶液中的溶解度很小,乙醇最好的處理方法是用過量飽和碳酸鈉溶液洗滌后分液,故答案為:催化劑和吸水劑;b。


 海淀黃岡名師導航系列答案
海淀黃岡名師導航系列答案 普通高中同步練習冊系列答案
普通高中同步練習冊系列答案科目:高中化學 來源: 題型:
【題目】NOx、SO2是常用的化工原料,含NOx、SO2的煙氣大量排放能造成嚴重的大氣污染。
(1)含NH3、NOx、SO2的煙氣在大氣中相互作用,產生的霧霾顆粒中有多種無機鹽,其中無機銨鹽主要是_____________(填化學式,只寫兩種)。
(2)SO2催化氧化反應2SO2(g)+O2(g)![]() 2SO3(g)的能量與反應進程如圖所示:
2SO3(g)的能量與反應進程如圖所示:

①該反應的正反應為____熱(填“放”或“吸”)反應。
②若該反應在恒溫恒容密閉容器中進行,能說明該 反應已達到化學平衡狀態的是____(填標號)。
A.SO2的v(正)=v(逆)
B.混合氣體中同時存在SO2、O2、SO3
C.容器內混合氣體密度不隨時間而變化
D.容器內混合氣體總壓強不再隨時間而變化
(3)Wang c H等研究發現用Fe2O3/CeO2作催化劑,可用乙烯脫除煙氣中SO2并回收單質硫。反應原理為:CH2=CH2+3SO2![]() 3S+2CO2+2H2O。某興趣小組同學設計實驗驗證該反應并檢驗產物中的CO2,實驗裝置(夾持裝置已略)如圖所示:
3S+2CO2+2H2O。某興趣小組同學設計實驗驗證該反應并檢驗產物中的CO2,實驗裝置(夾持裝置已略)如圖所示:
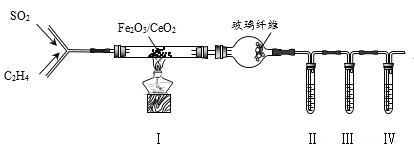
①實驗中所需SO2可由Cu與濃硫酸反應制取,該反應的化學方程式為________。
②已知:酸性KMnO4可將CH2=CH2氧化為CO2;裝置Ⅱ、Ⅲ中試劑均足量;裝置(Ⅰ)的尾氣中還含有未反應的SO2和CH2=CH2。檢驗CO2時,Ⅱ、Ⅲ、Ⅳ中盛放的試劑依次可以是_____(填標號)。
A.酸性KMnO4溶液、品紅溶液、澄清石灰水
B.NaOH溶液、酸性KMnO4溶液、澄清石灰水
C.Br2的H2O溶液、品紅溶液、澄清石灰水
D.Br2的CCl4溶液、酸性KMnO4溶液、澄清石灰水
(4)取用氨水脫除煙氣中SO2得到的副產品[只含(NH4)2SO4和NH4HSO4] 3.875g,與足量NaOH混合后加熱充分反應,共收集到氨氣1.232L(已折合為標準狀況),則該副產品中(NH4)2SO4和NH4HSO4的物質的量之比n[(NH4)2SO4]∶n(NH4HSO4)=______(寫出計算結果即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】右圖表示反應N2(g)+3H2(g)![]() 2NH3(g); ΔH=-92.2kJ/mol。 在某段時間t0~ t6中反應速率與反應過程的曲線圖,則氨的百分含量最高的一段時間是 ( )
2NH3(g); ΔH=-92.2kJ/mol。 在某段時間t0~ t6中反應速率與反應過程的曲線圖,則氨的百分含量最高的一段時間是 ( )

A、t0—t1 B t2—t3 C t3—t4 D t5—t6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海洋具有十分巨大的開發潛力,人們可以從海水中獲得多種物質.工業上進行海水淡化有多種方法.
(1)蒸餾法是歷史悠久,技術和工藝比較成熟的海水淡化方法,如圖1是海水蒸餾法裝置示意圖,儀器B的名稱是__________。

(2)圖2是膜分離技術進行淡化的原理示意圖,水分子可以透過淡化膜,而海水中其他各種粒子不能通過淡化膜,加壓后,右側海水中減少的是______(填字母)。
A.溶質質量 B.溶劑質量 C.溶質的物質的量濃度
Ⅱ.從海水中提取一些重要的化工產品的工藝流程如圖所示。

根據上述流程圖回答下列問題:
(3)標準狀況下22.4 L Cl2氣體發生反應②,轉移的電子數是________NA。
(4)過程③到過程⑤的變化為“Br-→Br2→Br-→Br2”,其目的是_______________。
(5)過程⑥⑦⑧⑨⑩中沒有涉及的化學反應類型是______。
A.分解反應 B.化合反應 C.復分解反應 D.置換反應
(6)寫出反應④與⑩的化學方程式
④________________________________________________;
⑩________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,將等量的氣體分別通入起始體積相同的密閉容器Ⅰ和Ⅱ中,使其發生反應,t0時容器Ⅰ中達到化學平衡,X、Y、Z的物質的量的變化如圖所示。則下列有關推斷正確的是( )
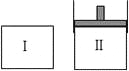
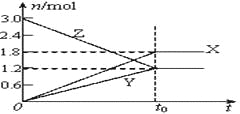
A. 該反應的化學方程式為:3X+2Y![]() 2Z
2Z
B. 若兩容器中均達到平衡時,兩容器的體積V(Ⅰ)<V(Ⅱ),則容器Ⅱ達到平衡所需時間小于t0
C. 若兩容器中均達到平衡時,兩容器中Z的物質的量分數相同,則Y為固態或液態
D. 若達平衡后,對容器Ⅱ升高溫度時,其體積增大,說明Z發生的反應為吸熱反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素X、Y、Z、W、R、Q原子序數依次增大。由這些元素組成的化合物甲、乙、丙、丁的0.1mol/L水溶液pH如下表,丙、丁為二元化合物。甲溶液逐滴滴入丙溶液中,先產生白色沉淀,后沉淀消失;乙的水溶液可除油污。下列說法一定正確的是

A. W和Q形成的化合物只含有離子鍵
B. Y和Z的氫化物沸點:Y<Z
C. 離子半徑:r(Q>r(R)>r(Z)
D. Y和Q氧化物的水化物酸性:Q>Y
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】500℃條件下,在恒容密閉容器中,充入1molNO2存在如下平2NO2(g)![]() N2O4(g) ,平衡后,向容器內再充入1molNO2,下列說法不正確的
N2O4(g) ,平衡后,向容器內再充入1molNO2,下列說法不正確的
A. 平衡向正反應方向移動 B. 平衡常數K增大
C. NO2的轉化率變大 D. 容器內氣體顏色先變深后變淺,最后比原來還要深
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于溶液的下列說法不正確的是( )
A. 某溫度下,Ba(OH)2溶液中Kw=10-12,向pH=8的該溶液中加入等體積pH=4的鹽酸,充分反應后,混合溶液的pH=6
B. 水電離出來的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-可能大量存在
C. 往0.1mol/LNH4Cl溶液中不斷加入NaOH固體,隨著NaOH的加入,![]() 不斷減小
不斷減小
D. 一定溫度下,氫氧化鈣達到溶解平衡,向此溶液中加入少量氧化鈣粉末(不考慮熱效應),則溶液中c(Ca2+)減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為驗證鹵素單質氧化性的相對強弱,某學習小組用下圖所示裝置進行實驗(夾持儀器已略去,氣密性已檢驗)。實驗過程:
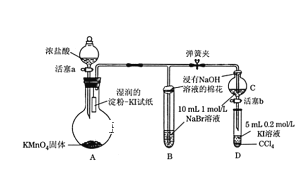
Ⅰ. 打開彈簧夾,打開活塞a,滴加濃鹽酸。
Ⅱ. 當B和C中的溶液都變為黃色時,夾緊彈簧夾。
Ⅲ. 當B中溶液由黃色變為棕紅色時,關閉活塞a。
Ⅳ.……
回答問題:
(1)A中產生黃綠色氣體,其電子式是_________。實驗室在加熱條件下制取該氣體的離子方程式為____________。
(2)驗證氯氣的氧化性強于碘單質的實驗現象是____________。
(3)C中溶液發生反應的離子方程式是_______________。
(4)過程Ⅲ實驗的目的:甲同學認為試管B的作用就是吸收尾氣,防止多余Cl2污染空氣,因此B中盛裝的最佳試劑應該為__________________________
乙同學經分析認為,B中溶液由黃色變為棕紅色,發生反應為Cl2+2NaBr=2NaCl+Br2,以此說明C中________,從而得出D中氧化I-的氧化劑必為_______,因此B裝置是必不可少的。
(5)過程Ⅳ為:打開活塞b,將少量C中溶液滴入D中,關閉活塞b,取下試管D震蕩,靜置,觀察到的現象為______________,發生反應的離子方程式為_____________________。
(6)氯、溴、碘單質的氧化性逐漸減弱的本質原因:同主族元素從上到下_________,得電子能力逐漸減弱。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com