
| A. | 乙烯和乙炔屬于不飽和烴,乙烷屬于飽和烴 | |
| B. | 乙烯和乙炔分子中所有原子都在同一平面上,乙烷分子中所有原子不都在同一平面上 | |
| C. | 乙烯和乙炔都能發生加成反應,乙烷不能發生加成反應 | |
| D. | 在發生加成反應時,乙烯和乙炔分子中的碳碳鍵全部斷裂 |
分析 A.飽和烴符合CnH2n+2,H原子減少時為不飽和烴;
B.乙烯為平面結構,乙炔為直線結構,而乙烷中C均為四面體構型;
C.雙鍵、三鍵可發生加成反應轉化為單鍵;
D.加成反應時,雙鍵、三鍵中的一個鍵不變.
解答 解:A.飽和烴符合CnH2n+2,H原子減少時為不飽和烴,則乙烯和乙炔屬于不飽和烴,乙烷屬于飽和烴,故A正確;
B.乙烯為平面結構,乙炔為直線結構,而乙烷中C均為四面體構型,則乙烯和乙炔分子中所有原子都在同一平面上,乙烷分子中所有原子不都在同一平面上,故B正確;
C.雙鍵、三鍵可發生加成反應轉化為單鍵,則乙烯和乙炔都能發生加成反應,乙烷不能發生加成反應,故C正確;
D.加成反應時,雙鍵、三鍵中的一個鍵不變,加成反應中碳碳鍵不能全部斷裂,故D錯誤;
故選D.
點評 本題考查有機物的結構與性質,為高頻考點,把握官能團與性質的關系、有機物的結構為解答的關鍵,側重分析與應用能力的考查,注意加成反應的判斷,題目難度不大.


科目:高中化學 來源: 題型:解答題
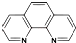 ),它能與Fe2+形成紅色配合物(如圖甲),該配離子中Fe2+與氮原子形成配位鍵共有6個.
),它能與Fe2+形成紅色配合物(如圖甲),該配離子中Fe2+與氮原子形成配位鍵共有6個.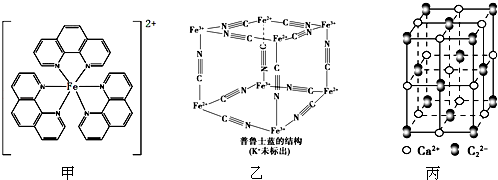
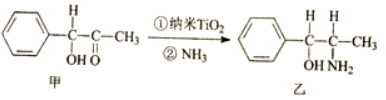
 ,其中σ鍵與π鍵數目之比為1:2.
,其中σ鍵與π鍵數目之比為1:2.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
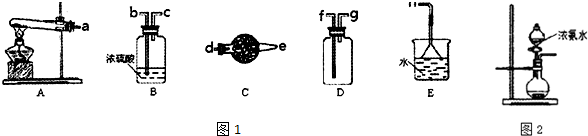
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
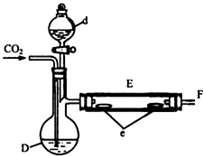 實驗室用如圖所示裝置制取溴化亞鐵.D和d中均盛有液溴,E為外套電爐絲的瓷管,e是兩只耐高溫的瓷皿,其中共盛有56g細鐵粉.實驗開始時先將干燥、純凈的CO2氣流通入D中,然后將鐵粉加熱至600℃~700℃,E管中反應開始.E中的反應為:2Fe+3Br2═2FeBr3,2FeBr3$\frac{\underline{\;\;△\;\;}}{\;}$2FeBr2+Br2↑,最后將d中液溴滴入100℃~120℃的D中,經過幾小時的連續反應,在鐵管的一端沉積有黃綠色鱗片狀溴化亞鐵80g.請回答:
實驗室用如圖所示裝置制取溴化亞鐵.D和d中均盛有液溴,E為外套電爐絲的瓷管,e是兩只耐高溫的瓷皿,其中共盛有56g細鐵粉.實驗開始時先將干燥、純凈的CO2氣流通入D中,然后將鐵粉加熱至600℃~700℃,E管中反應開始.E中的反應為:2Fe+3Br2═2FeBr3,2FeBr3$\frac{\underline{\;\;△\;\;}}{\;}$2FeBr2+Br2↑,最后將d中液溴滴入100℃~120℃的D中,經過幾小時的連續反應,在鐵管的一端沉積有黃綠色鱗片狀溴化亞鐵80g.請回答:| 實驗操作 | 實驗現象 | 氧化性強弱 |
| ① | 溶液呈血紅色 | ② |
| ③ | ④ | Cl2>Br2 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 大力發展以煤炭為原料的火力發電,促進經濟發展 | |
| B. | 在生產和生活中提倡使用節能技術和節能用具 | |
| C. | 開發新能源,代替傳統能源 | |
| D. | 提倡乘坐公交車、騎自行車或步行的方式出行 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 金屬 離子 | 氫氧化物開始沉淀的pH | 氫氧化物沉淀完全的pH |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2H2(g)+O2(g)=2H2O(l);△H=-142.9 kJ•mol-1 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)=H2O(l);△H=-285.8 kJ•mol-1 | |
| C. | 2H2+O2=2H2O;△H=-571.6 kJ•mol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g);△H=-285.8 kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 原子序數小于36的X、Y、Z、W四種元素,其中X形成的陽離子就是一個質子,Y原子基態時最外層電子數是其內層電子數的2倍,Z原子基態時2p原子軌道上有3個未成對的電子,W的原子序數為29.回答下列問題:
原子序數小于36的X、Y、Z、W四種元素,其中X形成的陽離子就是一個質子,Y原子基態時最外層電子數是其內層電子數的2倍,Z原子基態時2p原子軌道上有3個未成對的電子,W的原子序數為29.回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com