
| A. | 前20 min的平均反應速度$\overline v$(C)=0.1 mol/(L•min) | |
| B. | A的轉化率為50% | |
| C. | C的平衡濃度c(C)=4 mol/L | |
| D. | B的平衡濃度c(B)=1.0 mol/L |
分析 反應開始20min后達到平衡狀態,此時D的平衡濃度為0.5mol/L,則
2A(g)+3B(g)?4C(g)+D(g)
開始 2 3 0 0
轉化 1 1.5 2 0.5
平衡 1 1.5 2 0.5
結合v=$\frac{△c}{△t}$、轉化率=$\frac{轉化的量}{開始的量}$×100%、c=$\frac{n}{V}$計算.
解答 解:反應開始20min后達到平衡狀態,此時D的平衡濃度為0.5mol/L,則
2A(g)+3B(g)?4C(g)+D(g)
開始 2 3 0 0
轉化 1 1.5 2 0.5
平衡 1 1.5 2 0.5
A.前20 min的平均反應速度$\overline v$(C)=$\frac{2mol/L}{20min}$=0.1 mol/(L•min),故A正確;
B.A的轉化率為$\frac{1mol}{2mol}$×100%=50%,故B正確;
C.由上述分析可知C的平衡濃度c(C)=2 mol/L,故C錯誤;
D.B的平衡濃度c(B)=1.5 mol/L,故D錯誤;
故選CD.
點評 本題考查化學平衡的計算,為高頻考點,把握化學平衡三段法、轉化率計算等為解答的關鍵,側重分析與計算能力的考查,注意平衡濃度的判斷,題目難度不大.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 只要選擇適宜的條件,SO2和O2就能全部轉化為SO3 | |
| B. | 該反應達到平衡后,反應就停止了,即正逆反應速率為零 | |
| C. | 在達到平衡的體系中,充入O2,對化學平衡無影響 | |
| D. | 在工業合成SO3時,要同時考慮反應速率和反應所能達到的限度兩個方面的問題 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 第三周期元素的最高正化合價等于它所處的族序數 | |
| B. | 主族族序數與價電子數相同 | |
| C. | 非金屬元素在化合物中既可顯正價又可顯負價 | |
| D. | 所有非金屬元素的負化合價等于使原子達到8電子穩定結構所需得到的電子數 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
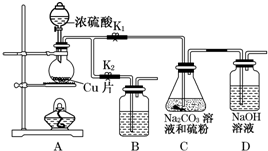
| 編號 | 1 | 2 | 3 | 4 |
| 溶液的體積/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2標準溶液的體積/mL | 19.99 | 19.98 | 17.13 | 20.03 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
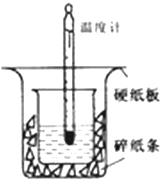 50ml0.50mol•L-1鹽酸與50mL0.55mol•L-1NaOH溶液在如下圖所示的裝置中進行中和反應.通過測定反應過程中放出的熱量可計算中和熱.
50ml0.50mol•L-1鹽酸與50mL0.55mol•L-1NaOH溶液在如下圖所示的裝置中進行中和反應.通過測定反應過程中放出的熱量可計算中和熱.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
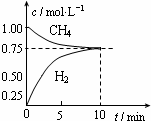 工業上制備合成氣的工藝主要是水蒸氣重整甲烷:CH4(g)+H2O(g)?CO(g)+3H2(g);△H=+206kJ/mol,一定條件下向體積為1L的密閉容器中充入1mol CH4和1mol H2O,測得CH4(g)和CO(g)的濃度隨時間變化曲線如圖所示,下列說法正確的是( )
工業上制備合成氣的工藝主要是水蒸氣重整甲烷:CH4(g)+H2O(g)?CO(g)+3H2(g);△H=+206kJ/mol,一定條件下向體積為1L的密閉容器中充入1mol CH4和1mol H2O,測得CH4(g)和CO(g)的濃度隨時間變化曲線如圖所示,下列說法正確的是( )| A. | 10min時用CH4表示的反應速率為0.075 mol•L-1•min-1 | |
| B. | 使用高效催化劑能夠增大CO的產率 | |
| C. | 該條件下反應的平衡常數為0.1875 | |
| D. | 升高溫度能使$\frac{c(C{H}_{4})}{c(CO)}$增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 50 mL 2 mol/L CaCl2溶液 | B. | 100 mL 2 mol/L NaCl溶液 | ||
| C. | 50 mL 4 mol/L CaCl2溶液 | D. | 100 mL 2 mol/L KClO3溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com