
 鍺(Ge)是典型的半導體元素,在電子、材料等領域應用廣泛.回答下列問題:
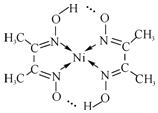
鍺(Ge)是典型的半導體元素,在電子、材料等領域應用廣泛.回答下列問題: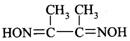 )常用于檢驗Ni2+:在稀氨水介質中,丁二酮肟與Ni2+反應可生成鮮紅色沉淀,其結構如圖所示.
)常用于檢驗Ni2+:在稀氨水介質中,丁二酮肟與Ni2+反應可生成鮮紅色沉淀,其結構如圖所示.分析 (1)Ge是32號元素,位于第四周期第IVA族,基態Ge原子核外電子排布式為[Ar]3d104s24p2;
(2)元素的非金屬性越強,吸引電子的能力越強,元素的電負性越大;
(3)根據中心原子的價層電子對數判斷雜化類型和空間結構;具有相同的原子數和價電子數的微粒互為等電子體;
(4)同周期從左到右第一電離能呈遞增趨勢,但是第IIA與IIIA族、第VA與第VIA族反常;
(5)單鍵中含有一個σ鍵,雙鍵中含有2個σ鍵;
(6)當共價鍵中共用電子對是由其中一原子獨自供應,另一原子提供空軌道時,此共價鍵屬于配位鍵.
解答 解:(1)Ge是32號元素,位于第四周期第IVA族,基態Ge原子核外電子排布式為1s22s22p63s23p63d104s24p2或[Ar]3d104s24p2,在最外層的4s能級上2個電子為成對電子,4p軌道中2個電子分別處以不同的軌道內,有2軌道未成對電子,
故答案為:4s24p2;2;
(2)元素非金屬性:Zn<C<O,元素的非金屬性越強,吸引電子的能力越強,元素的電負性越大,故電負性:O>C>Zn,
故答案為:O>C>Zn;
(3)BF3中B原子價層電子對數=3+$\frac{1}{2}$(3-3×1)=3,雜化類型為sp2,B原子周圍沒有孤電子對,則BF3的空間構型為平面三角形;具有相同的原子數和價電子數的微粒互為等電子體,與互為等電子體的離子為 CO32-;
故答案為:sp2;平面三角形; CO32-;
(4)同周期從左到右第一電離能呈遞增趨勢,但是第IIA與IIIA族、第VA與第VIA族反常,所以硼、氧、氟、氮中第一電離能由大到小的順序是:F>N>O>B;
故答案為:F>N>O>B;
(5)丁二酮肟(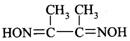 )分子中含有13個單鍵和2個雙鍵,單鍵中含有一個σ鍵,雙鍵中含有2個σ鍵,所以1mol該物質中含有σ鍵15NA個;
)分子中含有13個單鍵和2個雙鍵,單鍵中含有一個σ鍵,雙鍵中含有2個σ鍵,所以1mol該物質中含有σ鍵15NA個;
故答案為:σ鍵;15NA;
(6)當共價鍵中共用電子對是由其中一原子獨自供應,另一原子提供空軌道時,此共價鍵屬于配位鍵,圖中氮鎳之間形成的共價鍵屬于配位鍵;
故答案為:配位鍵.
點評 本題考查了物質結構與性質,涉及核外電子排布、化學鍵、電負性、雜化方式、配位鍵等,題目難度中等,側重于考查學生對基礎知識的綜合應用能力,注意把握雜化類型的判斷方法.


科目:高中化學 來源: 題型:選擇題
| A. | c (NH3•H2O)>c (NH4+)>c (H+)>c (OH-) | B. | c (NH4+)>c (NH3•H2O)>c (OH-)>c (H+) | ||
| C. | c (NH3•H2O)>c (NH4+)=c (OH-)>c (H+) | D. | c (NH3•H2O)>c (OH-)>c (NH4+)>c (H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 圖中新月形分子和環狀分子“組合”在一起,銅離子起關鍵作用 | |
| B. | 利用此方式可以合成新分子,同時也可能創造一種全新“機械鍵” | |
| C. | 在創造新分子技術中,銅離子是唯一可以借助的金屬離子 | |
| D. | 此技術可以“互鎖”合成  分子,甚至成更復雜的分子 分子,甚至成更復雜的分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用潔凈的鉑絲蘸取少量溶液在酒精燈火焰上灼燒,火焰呈黃色,則該溶液中一定不含K+ | |
| B. | 向無色溶液中加入鹽酸酸化的BaCl2溶液有白色沉淀出現,則該溶液中一定含有SO42- | |
| C. | 向無色溶液中加入鹽酸產生能使澄清石灰水變渾濁的氣體,則該溶液中一定含有CO32- | |
| D. | 向某溶液中加入KSCN溶液無現象,再滴入少量H2O2,呈血紅色,則該溶液中一定含有Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
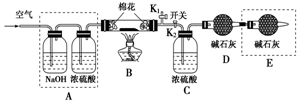 為探究所得的水合堿式碳酸鎂[mMgCO3•nMg(OH)2•x
為探究所得的水合堿式碳酸鎂[mMgCO3•nMg(OH)2•x查看答案和解析>>
科目:高中化學 來源: 題型:解答題
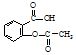 )具有解熱鎮痛作用(選填“解熱鎮痛”或“抗菌消炎”),必須密閉干燥存儲以防止發生水解,在酸性條件下阿司匹林水解生成乙酸和
)具有解熱鎮痛作用(選填“解熱鎮痛”或“抗菌消炎”),必須密閉干燥存儲以防止發生水解,在酸性條件下阿司匹林水解生成乙酸和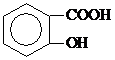 (寫出結構簡式).
(寫出結構簡式).查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
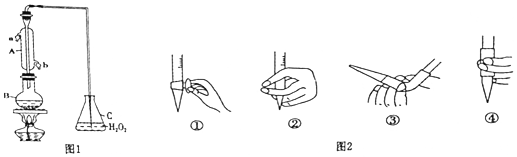
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯的三氯代物一共有 5 種 | |
| B. | 乙烯和乙酸均能發生加成反應 | |
| C. | 乙烷通入氯水中能發生取代反應 | |
| D. | 淀粉和纖維素都屬于天然高分子化合物 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com