
 (1)1mol氫氣在氯氣中充分燃燒生成氯化氫氣體時放出184.6kJ的熱量,試寫出對應的熱化學方程式H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1.標準狀況下11.2L氫氣在氯氣中充分燃燒放出的熱量是92.3kJ.
(1)1mol氫氣在氯氣中充分燃燒生成氯化氫氣體時放出184.6kJ的熱量,試寫出對應的熱化學方程式H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1.標準狀況下11.2L氫氣在氯氣中充分燃燒放出的熱量是92.3kJ.分析 (1)依據熱化學方程式的書寫原則和注意問題寫出,標注聚集狀態和焓變,標準狀況下11.2L氫氣物質的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,結合熱化學方程式計算;
(2)△H=生成物能量和-反應物能量和,從圖象可見,反應物的能量低于生成物,反應吸熱,據此分析.
解答 解:(1)1mol氫氣在氯氣中充分燃燒生成氯化氫氣體時放出184.6kJ的熱量,對應的熱化學方程式為:H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1,標準狀況下11.2L氫氣物質的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,反應放熱=184.6 kJ•mol-1×0.5mol=92.3KJ,
故答案為:H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1;92.3;
(2)①反應物的能量高于生成物,1mol氣體A和1mol氣體B具有的能量比1mol氣體C和1mol氣體D具有的總能量一定高,故答案為:大于;
②△H=生成物能量和-反應物能量和<0,反應放熱,△H=反應物活化能-生成物活化能=(E1-E2)kJ/mol,故答案為:放熱;(E1-E2).
點評 本題通過圖象分析反應放熱還是吸熱與反應物生成物能量高低的關系,以及通過活化能計算焓變的方法,題目難度不大.


科目:高中化學 來源: 題型:填空題
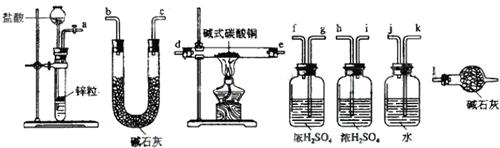
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
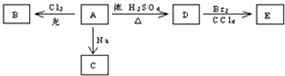 化合物A(C4H10O)是一種有機溶劑.A可以發生如圖變化:
化合物A(C4H10O)是一種有機溶劑.A可以發生如圖變化: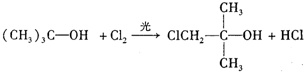 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2種 | B. | 3種 | C. | 4種 | D. | 5種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 物質的量比為11:16 | B. | 密度比為16:11 | ||
| C. | 體積比為16:11 | D. | 體積比為11:16 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 12553I 原子核內中子數為53 | |
| B. | 12553I原子核外電子數為72 | |
| C. | 12553I 和12753I互為同位素 | |
| D. | 12553I代表有53個質子和125個中子的碘原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若體積相等,則密度相等 | B. | 若質量相等,則質子數相等 | ||
| C. | 若分子數相等,則體積相等 | D. | 若原子數相等,則電子數相等 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com