
 (1,3-環己二烯)的各步反應方程式
(1,3-環己二烯)的各步反應方程式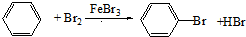
 +3H2$\stackrel{一定條件下}{→}$
+3H2$\stackrel{一定條件下}{→}$
 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$ +H2O+NaBr
+H2O+NaBr +Br2→
+Br2→
 +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$ +2NaBr+2H2O.
+2NaBr+2H2O. 分析 在FeBr3作催化劑條件下,苯和液溴發生取代反應生成溴苯,溴苯和氫氣在一定條件下發生加成反應生成1-溴環己烷,1-溴環己烷和NaOH的醇溶液加熱生成環己烯,環己烯和溴發生加成反應生成1,2-二溴環己烷,1,2-二溴環己烷和NaOH的醇溶液加熱發生消去反應生成 ,據此分析解答.
,據此分析解答.
解答 解:在FeBr3作催化劑條件下,苯和液溴發生取代反應生成溴苯,溴苯和氫氣在一定條件下發生加成反應生成1-溴環己烷,1-溴環己烷和NaOH的醇溶液加熱生成環己烯,環己烯和溴發生加成反應生成1,2-二溴環己烷,1,2-二溴環己烷和NaOH的醇溶液加熱發生消去反應生成 ,涉及的反應方程式分別為:
,涉及的反應方程式分別為: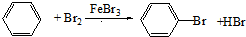 、
、 +3H2$\stackrel{一定條件下}{→}$
+3H2$\stackrel{一定條件下}{→}$ 、
、 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$ +H2O+NaBr、
+H2O+NaBr、 +Br2→
+Br2→ 、
、 +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$ +2NaBr+2H2O,
+2NaBr+2H2O,
故答案為: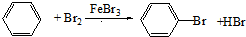 ;
; +3H2$\stackrel{一定條件下}{→}$
+3H2$\stackrel{一定條件下}{→}$ ;
; +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$ +H2O+NaBr;
+H2O+NaBr; +Br2→
+Br2→ ;
; +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$ +2NaBr+2H2O.
+2NaBr+2H2O.
點評 本題以有機合成為載體考查化學方程式的書寫,明確官能團及其性質關系是解本題關鍵,注意物質發生反應時的反應條件,反應物相同其條件不同會導致產物不同,注意溴代烷發生消去反應、水解反應條件的區別,題目難度不大.


科目:高中化學 來源: 題型:選擇題
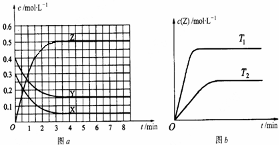
| A. | 該反應的正反應是放熱反應 | |
| B. | T0時,該反應的平衡常數為$\frac{1}{3}$ | |
| C. | 反應時各物質的反應速率關系為:2v (X)=2v (Y)=v (Z) | |
| D. | 圖a中反應達到平衡時,Y的轉化率為37.5% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 溴水 | B. | 酸性高錳酸鉀溶液 | ||
| C. | 溴的CCl4溶液 | D. | 銀氨溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
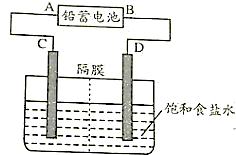
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省高二上第三次月考化學卷(解析版) 題型:填空題
(本題滿分18分)二甲 醚(CH3OCH3)是一種應用前景廣闊的清潔燃料,以CO和H2為原料生產二甲醚主要發生以下三個反應:
醚(CH3OCH3)是一種應用前景廣闊的清潔燃料,以CO和H2為原料生產二甲醚主要發生以下三個反應:
編號 | 熱化學方程式 | 化學平衡常數 |
① | CO(g)+2H2(g) | K1 |
② | 2CH3OH(g) | K2 |
③ | CO(g)+H2O(g) | K3 |
回答下列問題:
(1)已知反應①中的相關的化學鍵鍵能數據如下:
化學鍵 | H﹣H | C﹣O | C=O | H﹣O | C﹣H |
E/(kJ.mol﹣1) | 436 | 343 | 1076 | 465 | 413 |
由上述數據計算△H1= ;
(2)該工藝的總反應為3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)△H,該反應△H= ,化學平衡常數K= (用含K1、K2、K3的代數式表示);
CH3OCH3(g)+CO2(g)△H,該反應△H= ,化學平衡常數K= (用含K1、K2、K3的代數式表示);
(3)下列措施中,能提高CH3OCH3產率的有 ;
A.分離出二甲醚 B.升高溫度
C.改用高效催化劑 D.增大壓強
(4)工藝中反應①和反應②分別在不同的反應器中進行,無反應③發生.該工藝中反應③的發生提高了CH3OCH3的產率,原因是 ;
(5)以n(H2)/n(CO)=2 通入1L的反應器中,一定條件下發生反應:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g)△H,其CO的平衡轉化率隨溫度、壓強變化關系如圖所示.下列說法正確的是 ;
CH3OCH3(g)+H2O(g)△H,其CO的平衡轉化率隨溫度、壓強變化關系如圖所示.下列說法正確的是 ;
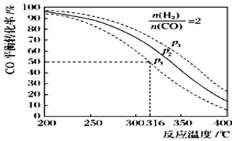
A.該反應的△H>0
B.若在p2和316℃時反應達到平衡,則CO的轉化率小于50%
C.若在p3和316℃時反應達到平衡,H2的轉化率等于50%
D.若在p3和316℃時,起始時n(H2)/n(CO)=3,則達平衡時CO的轉化率大于50%
E.若在p1和200℃時,反應達平衡后保持溫度和壓強不變,再充入2mol H2和1mol CO,則平衡時二甲醚的體積分數增大
(6)某溫度下,將8.0mol H2和4.0mol CO充入容積為2L的密閉容器中,發生反應:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g),反應達平衡后測得二甲醚的體積分數為25%,則該溫度下反應的平衡常數K= .
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省高二上10月月考化學試卷(解析版) 題型:選擇題
下表是25℃時某些鹽的濃度積常數和弱酸的電離平衡常數,下列說法正確的是( )
化學式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
Ksp或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
A.相同濃度CH3COONa和NaClO的混合液中,各離子濃度的大小關系是
c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.碳酸鈉溶液中滴加少量氯水的離子方程式H2O+2CO32-+Cl2=2HCO3-+Cl-+ClO-
C.向0.1mol/LCH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=9:5,此時溶液pH=5
D.向濃度均為1×10-3mol/L的KCl和K2CrO4混合液中滴加1×10-3mol/L的AgNO3溶液,CrO42-先形成沉淀
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省高二上第一次月考化學卷(解析版) 題型:選擇題
對于可逆反應N2(g)+3H2(g) 2NH3(g) △H<0,下列研究目的和示意圖相符的是
2NH3(g) △H<0,下列研究目的和示意圖相符的是
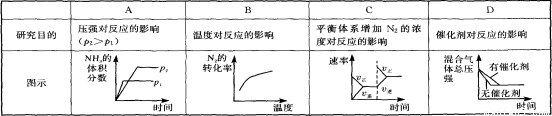
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com