
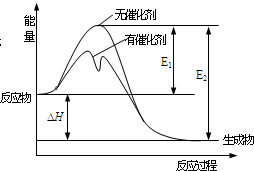
 2SO2(g)+O2(g)?2SO3(g)反應過程中能量變化如圖所示(圖中E1表示正反應的活化能,E2表示逆反應的活化能).下列有關敘述正確的是( )
2SO2(g)+O2(g)?2SO3(g)反應過程中能量變化如圖所示(圖中E1表示正反應的活化能,E2表示逆反應的活化能).下列有關敘述正確的是( )| A. | 該反應為吸熱反應 | |
| B. | 升高溫度,不影響活化分子百分數 | |
| C. | 使用催化劑使該反應的反應熱發生改變 | |
| D. | E1-E2=△H |
分析 A.圖象分析反應物能量高于生成物能量,反應是放熱反應;
B.升高溫度,活化分子百分數增大,單位體積內的活化分子數增大;
C.催化劑對反應的焓變無影響;
D.圖象分析反應焓變=E1-E2.
解答 解:A.圖象分析反應物能量高于生成物能量,反應是放熱反應,故A錯誤;
B.升高溫度,活化分子百分數增大,單位體積內的活化分子數增大,所以反應速率增大,故B錯誤;
C.催化劑對反應的始態和狀態無響應,只改變活化能,則對反應的焓變無影響,故C錯誤;
D.△H=斷鍵吸收的能量-成鍵放出的能量=E1-E2,故D正確.
故選D.
點評 本題考查了化學變化過程中能量變化的分析的,主要是活化能概念的理解應用,掌握圖象分析方法是關鍵,題目較簡單.


科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol•L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 0.1 mol•L-1NaHCO3溶液與0.1 mol•L-1NaOH溶液等體積混合:c(Na+)=2c(CO32-)+c(HCO3-)+2c(H2CO3) | |
| C. | 0.1 mol•L-1NaHCO3溶液與0.2 mol•L-1NaOH溶液等體積混合:c(Na+)>c(OH-)>0.05 mol•L-1>c(CO32-)>c(HCO3-) | |
| D. | 0.2 mol•L-1NaHCO3溶液與0.1 mol•L-1NaOH溶液等體積混合:c(CO32-)+c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷與氯氣混合后光照反應;乙烯使酸性高錳酸鉀溶液褪色 | |
| B. | 乙烯與溴的四氯化碳溶液反應;苯與氫氣在一定條件下反應生成環己烷 | |
| C. | 苯滴入濃硝酸和濃硫酸的混合液中,有油狀物生成; 乙烯與水生成乙醇的反應 | |
| D. | 在苯中滴入溴水,溴水褪色;乙烯自身生成聚乙烯的反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 序號 | 第一組 | 第二組 | 第三組 | 第四組 |
| t/℃ | 30 | 40 | 50 | 80 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| X | Y | ||
| Z | W |
| A. | W的原子半徑最大 | |
| B. | Z與X形成的化合物難溶于水 | |
| C. | Y的單質不能與水反應 | |
| D. | Z元素的氧化物對應水化物的酸性一定弱于W的氧化物對應水化物的酸性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
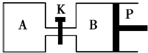 如圖所示的裝置中發生反應2A2(g)+B2(g)?2C(g)△H=-a kJ/mol(a>0),已知P是可自由滑動的活塞.在相同溫度時關閉K,向容積相同的A、B容器中分別都充入2mol A2和1mol B2氣體.兩容器分別在500℃達平衡時,A中C的濃度為c1 mol/L,放出熱量b kJ,B中C的濃度為c2 mol/L,放出熱量c kJ.下列說法中正確的是( )
如圖所示的裝置中發生反應2A2(g)+B2(g)?2C(g)△H=-a kJ/mol(a>0),已知P是可自由滑動的活塞.在相同溫度時關閉K,向容積相同的A、B容器中分別都充入2mol A2和1mol B2氣體.兩容器分別在500℃達平衡時,A中C的濃度為c1 mol/L,放出熱量b kJ,B中C的濃度為c2 mol/L,放出熱量c kJ.下列說法中正確的是( )| A. | 500℃達平衡時有:c1>c2 | |
| B. | 500℃達平衡時有:a>b>c | |
| C. | 達平衡后打開K,容器B的體積將減小 | |
| D. | 此反應的平衡常數隨溫度升高而增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
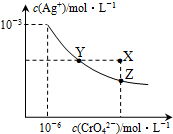 t℃時,AgCl的Ksp=2×10-10;Ag2CrO4是一種橙紅色固體,在水中的沉淀溶解平衡曲線如圖所示.下列說法正確的是( )
t℃時,AgCl的Ksp=2×10-10;Ag2CrO4是一種橙紅色固體,在水中的沉淀溶解平衡曲線如圖所示.下列說法正確的是( )| A. | 在t℃時,AgCl的溶解度大于Ag2CrO4 | |
| B. | 在t℃時,Ag2CrO4的Ksp=1×10-12 | |
| C. | 在飽和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y點到X點 | |
| D. | 在t℃時,用AgNO3標準溶液滴定20mL未知濃度的KCl溶液,不能采用K2CrO4溶液為指示劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
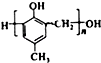 ,化合物C和化合物N的合成路線如下:
,化合物C和化合物N的合成路線如下: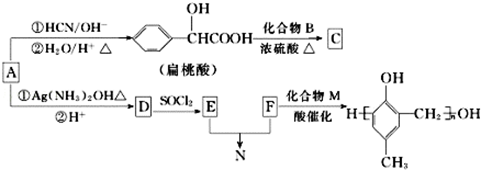
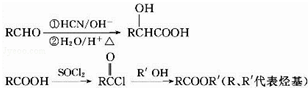
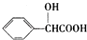
 ,D的含氧官能團的名稱是羧基.
,D的含氧官能團的名稱是羧基. .
.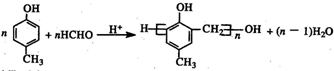 .
.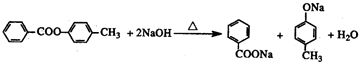 .
. )有多種同分異構體.其中含有三個取代基,能與FeCl3溶液發生顯色反應,也能與NaHCO3溶液反應放出氣體的同分異構體共有10種,寫出符合條件的三個取代基不相鄰的一種同分異構體的結構簡式
)有多種同分異構體.其中含有三個取代基,能與FeCl3溶液發生顯色反應,也能與NaHCO3溶液反應放出氣體的同分異構體共有10種,寫出符合條件的三個取代基不相鄰的一種同分異構體的結構簡式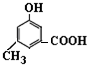 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
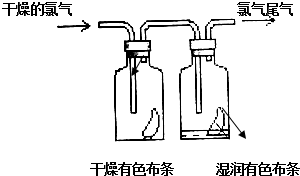 (1)如圖所示,將氯氣依次通過盛有干燥有色布條的廣口瓶和盛有濕潤有色布條的廣口瓶,可觀察到的現象是干燥的有色布條無明顯現象,潮濕的有色布條褪色.
(1)如圖所示,將氯氣依次通過盛有干燥有色布條的廣口瓶和盛有濕潤有色布條的廣口瓶,可觀察到的現象是干燥的有色布條無明顯現象,潮濕的有色布條褪色.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com