
(本題16分)工業上利用CO2和H2在一定條件下反應合成甲醇。
(1)已知在常溫常壓下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
②2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
寫出甲醇不完全燃燒生成一氧化碳和液態水的熱化學方程式:____________ ________
(2)甲醇脫氫可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡轉化率隨溫度變化曲線如下圖所示。回答下列問題:
HCHO(g)+H2(g),甲醇的平衡轉化率隨溫度變化曲線如下圖所示。回答下列問題:
①脫氫反應的△H_____0,600K時,Y點甲醇的υ(正) _____υ(逆)(填“>”或“<”)
②從Y點到X點可采取的措施是_______________________________________________。
③有同學計算得到在t1K時,該反應的平衡常數為8.1mol·L-1。你認為正確嗎?請說明理由__________________________________________________________________________。
(3)納米級Cu2O由于具有優良的催化性能而受到關注。在相同的密閉容器中,使用不同方法制得的Cu2O(Ⅰ)和(Ⅱ)分別進行催化CH3-OH的脫氫實驗:
CH3OH(g) HCHO(g)+H2(g)
HCHO(g)+H2(g)
CH3OH的濃度(mol·L-1)隨時間t (min)變化如下表:
| 序號 | 溫度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
(1)CH3OH(l)+ O2(g) = CO(g) + 2H2O(l) ΔH=﹣442.8 kJ∕mol (2分)
(2)①> (2分)②< (2分)
②降低溫度和增大壓強(2分)
③不正確(1分)。因為當CH3OH的起始濃度不同時,其轉化率就不等于90%。(1分)
(3)7.0×10-5 mol·L-1 min-1(2分) <(1分) <(1分)
(4)CH3-OH + 8OH- + 6e- = CO32- + 6H2O (2分)
解析試題分析:
(1)根據題意,先寫出甲醇不完全燃燒生成一氧化碳和液態水的化學方程式,標明狀態,再根據蓋斯定律求算焓變。
(2)①由坐標圖可知,隨著溫度的升高,甲醇的平衡轉化率在不斷地增大,即是溫度升高,平衡向正反應方向移動,所以焓變大于0;②Y點在曲線的上方,在該溫度下,平衡轉化率應比Y點小,所以平衡當向逆進行,才能達到X點,所以正反應速率小逆反應速率;可以采用降溫或增大壓強的方法;③不正確,起始濃度不一樣,轉化率就不同了。
(3)審清題意“實驗①的前20 min,ν(H2)”,ν(H2)=(0.050-0.0486)mol·L-1/20min
;該反應是吸熱反應,比較實驗①和實驗②達到平衡所需要的時間,便可判斷溫度的高低和催化劑的催化效果;
(4)負極發生的是氧化反應,所以先把這一部分CH3-OH -6e- → CO32-寫出來,因為電解質溶液是堿性的,C以CO32-存在,由電荷守恒可知,左邊當再加上OH-,右邊加上H2O,配平就可以了。
考點:熱化學方程式的書寫;影響化學平衡的因素;化學平衡常數的應用;化學反應速率的計算;電化學電極反應式的書寫。


科目:高中化學 來源: 題型:單選題
下列關于判斷過程的方向的說法正確的是( )
| A.所有自發進行的化學反應都是放熱反應 |
| B.高溫高壓下可以使石墨轉化為金剛石是自發的化學反應 |
| C.由能量判據和熵判據組合而成的復合判據,將更適合于所有的過程 |
| D.同一物質的固、液、氣三種狀態的熵值相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)工業上利用CO和水蒸氣在一定條件下發生反應制取氫氣:
①CO(g)+H2O(g)  CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
某小組研究在相同溫度下該反應過程中的能量變化。他們分別在體積均為V L的兩個恒溫恒容密閉容器中加入一定量的反應物,使其在相同溫度下發生反應。相關數據如下:
| 容器編號 | 起始時各物質物質的量/mol | 達到平衡的時間/min | 達平衡時體系能量的變化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 4 | 0 | 0 | t1 | 放出熱量:32.8 kJ | |
| ② | 2 | 8 | 0 | 0 | t2 | 放出熱量:Q | |


查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(共12分)(1)火箭推進器中盛有強還原劑液態肼(N2H4)和強氧化劑液態雙氧水。當把0.4mol液態肼和0.8mol H2O2混合反應,生成氮氣和水蒸氣,放出257.7kJ的熱量(相當于25℃、101 kPa下測得的熱量)。
①反應的熱化學方程式為 。
②又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。則16g液態肼與液態雙氧水反應生成液態水時放出的熱量是 kJ。
③此反應用于火箭推進,除釋放大量熱和快速產生大量氣體外,還有一個很大的優點是 。
(2)蓋斯定律在生產和科學研究中有很重要的意義。有些反應的反應熱雖然無法直接測得,但可通過間接的方法測定。現根據下列3個熱化學反應方程式:
Fe2O3(s)+3CO(g)="=" 2Fe(s)+3CO2(g) △H=—24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=—47.4kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
寫出CO氣體還原FeO固體得到Fe 固體和CO2氣體的熱化學反應方程式:
_________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(4分)拆開1mol氣態物質中某種共價鍵需要吸收的能量,就是該共價鍵的鍵能。下表是某些共價鍵的鍵能:
| 共價鍵 | H-H | O=O | H-O |
| 鍵能/kJ ·mol-1 | 436 | 498 | X |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 反應過程的能量變化如圖所示。已知l mol SO2(g)氧化為1 molSO3 (g)的
反應過程的能量變化如圖所示。已知l mol SO2(g)氧化為1 molSO3 (g)的 。請回答下問題;
。請回答下問題;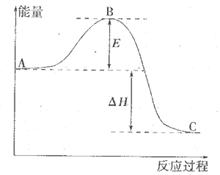
(1)E表示___________________;E的大小對該反應的反應熱__________(填“有”或“無”)影響。
(2)該反應通常用V2O5作催化劑,加V2O5會使圖中△H___________(填“變大”、“變小”或“不變”),理由是________。
(3)已知單質硫的燃燒熱為296 kJ·mol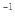 ,計算由S(s)生成2mol SO3(g)的△H =________________。
,計算由S(s)生成2mol SO3(g)的△H =________________。
(4)在一定條件下向容積為2L的容器中通入4molSO2和3molO2,充分反應達平衡后,SO3的體積分數為1/3。若在相同的條件下向容積為2L的容器中通入amolSO2和,bmolSO3,和cmol,反應向逆反應方向進行且達到平衡時SO3的體積分數也為1/3。則c的取值范圍為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(15分)
化合物AX3和單質X2在一定條件下反應可生成化合物AX5。回答下列問題:
(1)已知AX3的熔點和沸點分別為-93.6 ℃和76 ℃,AX5的熔點為167 ℃。室溫時AX3與氣體X2反應生成lmol AX5,放出熱量123.8 kJ。該反應的熱化學方程式為 。
(2)反應AX3(g)+X2(g) AX5(g)在容積為10 L的密閉容器中進行。起始時AX3和X2均為0.2 mol。反應在不同條件下進行,反應體系總壓強隨時間的變化如圖所示。
AX5(g)在容積為10 L的密閉容器中進行。起始時AX3和X2均為0.2 mol。反應在不同條件下進行,反應體系總壓強隨時間的變化如圖所示。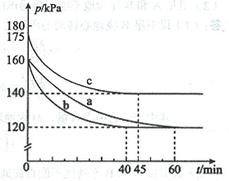
①列式計算實驗a從反應開始至達到平衡時的反應速率 v(AX5)= 。
②圖中3組實驗從反應開始至達到平衡時的反應速率v(AX5)由大到小的次序為 (填實驗序號);與實驗a相比,其他兩組改變的實驗條件及判斷依據是:b 、
c 。
③用p0表示開始時總壓強,p表示平衡時總壓強,α表示AX3的平衡轉化率,則α的表達式為
;實驗a和c的平衡轉化率:αa為 、αc為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)2013年12月2日,我國在西昌衛星發射中心用“長征三號甲”運載火箭將“嫦娥三號”探月衛星成功送入太空,進一步向廣寒宮探索。“長征三號甲”是三級液體助推火箭,一、二級為常規燃料,常規燃料通常指以肼(N2H4)為燃料,以二氧化氮做氧化劑。
Ⅰ.常規燃料通常指以肼(N2H4)為燃料,以二氧化氮做氧化劑。但有人認為若用氟氣代替二氧化氮作氧化劑,反應釋放的能量更大(兩者反應生成氮氣和氟化氫氣體)。
已知:①N2H4(g)+O2(g)=N2(g)+2H2O(g) △H = -543kJ·mol-1
②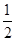 H2(g)+
H2(g)+ 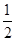 F2(g) = HF(g) △H = -269kJ·mol-1
F2(g) = HF(g) △H = -269kJ·mol-1
③H2(g)+ 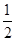 O2(g) = H2O(g) △H = -242kJ·mol-1
O2(g) = H2O(g) △H = -242kJ·mol-1
請寫出肼和氟氣反應的熱化學方程式:_____________________________。
Ⅱ.氧化劑二氧化氮可由NO和 O2生成,已知在2 L密閉容器內,800 ℃時反應:
2NO(g)+O2(g) 2NO2(g) ΔH 的體系中,n(NO)隨時間的變化如表:
2NO2(g) ΔH 的體系中,n(NO)隨時間的變化如表:
| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
| n(O2)(mol) | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)在焙燒爐中發生反應:
①Fe2O3(s)+3C(s) ===2Fe(s)+3CO(g) ΔH=-492.7 kJ·mol-1
②3CO(g)+Fe2O3(s) ===2Fe(s)+3CO2(g) ΔH=+25.2 kJ·mol-1
則2Fe2O3(s)+3C(s) ===4Fe(s)+3CO2(g) ΔH= kJ·mol-1。
(2)天然氣(以甲烷計)在工業生產中用途廣泛。甲烷蒸汽轉化法制H2的主要轉化反應如下:
CH4(g)+H2O(g) ===CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+2H2O(g) ===CO2(g)+4H2(g) ΔH=+165.0 kJ·mol-1
上述反應所得原料氣中的CO能使氨合成催化劑中毒,必須除去。工業上常采用催化劑存在下CO與水蒸氣反應生成易除去的CO2,同時又可制得等體積的氫氣的方法。此反應稱為一氧化碳變換反應,該反應的熱化學方程式是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com