
在一定溫度下的定容密閉容器中,下列情況能表明可逆反應:H2(g)+I2(g) 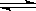 2HI(g)已達平衡的是
2HI(g)已達平衡的是
A.H2的生成速率與I2的生成速率相等
B.若單位時間內生成n mol H2的同時生成2n mol HI
C.H2、I2、HI的濃度相等
D.反應容器內的壓強不隨時間的變化而變化
科目:高中化學 來源:2016屆湖南省高三9月月考試化學試卷(解析版) 題型:選擇題
已知下列反應的平衡常數:①H2(g)+S(s)?H2S(g)K1 ②S(s)+O2(g)?SO2(g) K2則相同溫度下,反應H2+SO2?O2+H2S的平衡常數為
A.K1+K2 B.K1﹣K2 C.K1×K2 D.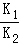
查看答案和解析>>
科目:高中化學 來源:2014-2015學年上海市高三第一學期第一次月考化學試卷(解析版) 題型:計算題
(本題共14分)中學化學中有許多與氮有關的反應。閱讀材料,回答問題。
1.氨氣和氧氣在催化劑存在下的反應方程式為4NH3十5O2→4NO+6H2O完成下列計算:
①生成1molNO消耗氧氣的體積為 L(標準狀況)。
②5 mol NH3和5 molO2反應生成4 molNO,過量的氨溶于產物水中成為氨水,所得氨水的密度為0.75g/ml,則該氨水的物質的量濃度為_____mol/L。
③.如果沒有催化劑,氨氧化生成NO的同時也生成氮氣:4NH3十3O2→2N2+6H2O。若4 mol NH3和4 molO2恰好完全反應,則產物氣體中NO的物質的量為_____ mol。
2.已知真空管中反應2NO2 N2O4,現向一真空管中充入4L標況下的NO2 氣體:
N2O4,現向一真空管中充入4L標況下的NO2 氣體:
① 若在上述反應中有50% NO2的轉化為N2O4,所得混合氣的平均摩爾質量為______g/mol
若在上述反應中有50% NO2的轉化為N2O4,所得混合氣的平均摩爾質量為______g/mol (保留一位小數)。
(保留一位小數)。
② 將4LNO2通過真空管反應后,恢復到原狀況,得到氣體3L,其中NO2為_______L。
將4LNO2通過真空管反應后,恢復到原狀況,得到氣體3L,其中NO2為_______L。
3.各種氮氧化物(NO、NO2)是主要的大氣污染物之一,治理氮氧化物(NOX)廢氣的方法之一是用NaOH溶液進行吸收,其反應原理可表示如下:
NO2+NO+2NaOH→2NaNO2+H2O 2NO2+2NaOH→ NaNO2+NaNO3+H2O
現有一NO與NO2的混合氣體,將其通入50mL 2mol/L的NaOH溶液中,恰好完全吸收,測得溶液中含有NO3― 0.02mol。
①所得溶液中NaNO2的物質的量為 mol;②混合氣體中V(NO):V(NO2)= 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北正定中學高二上學期第一次聯考化學試卷(解析版) 題型:選擇題
若溶液中由水電離產生的c(OH-)=1×10-14mol·L-1,滿足此條件的溶液中一定可以大量共存的離子組是
A.Al3+ Na+ NO3- Cl- B.K+ Na+ Cl- NO3-
C.K+ Na+ Cl- AlO2- D.K+ NH4+ SO42- NO3-
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省邯鄲市高二上第一次月考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.HCl溶液中無OH-
B.NaOH溶液中無H+
C.NaCl溶液中既無OH-,也無H+
D.常溫下,任何物質的稀溶液中都有H+和OH-,且Kw=c(H+)·c(OH-)=10-14
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北大名縣第一中學高二上學期第一次月考試化學試卷(解析版) 題型:選擇題
在容積為2升的密閉容器中,有反應:mA(g)+nB(g) 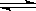 pC(g)+qD(g),經過5分鐘達到平衡,此時,各物質的變化為:A減少了amol·L-1,B的平均反應速度VB=
pC(g)+qD(g),經過5分鐘達到平衡,此時,各物質的變化為:A減少了amol·L-1,B的平均反應速度VB=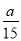 mol·L-1·min-1,C增加了
mol·L-1·min-1,C增加了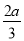 mol·L-1,這時,若增加系統壓強,發現A與C的百分含量不變,則m︰n︰p︰q為
mol·L-1,這時,若增加系統壓強,發現A與C的百分含量不變,則m︰n︰p︰q為
A.1︰1︰1︰1 B.1︰3︰2︰2
C.1︰3︰2︰1 D.3︰1︰2︰2
查看答案和解析>>
科目:高中化學 來源:2016屆浙江省高三上學期第一次模擬考試化學試卷(解析版) 題型:填空題
(8分)丙烯是重要的化工原料,一定條件下可發生下列轉化:

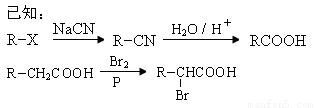
回答下列問題:
(1)以下化合物中含有羧基的是 。
A.化合物B B.化合物C C.化合物D D.化合物E
(2)上述反應中未涉及的反應類型是 。
A.取代反應 B.加成反應 C.還原反應 D.加聚反應
(3)寫出含碳數最少且與D互為同系物的有機物的結構簡式___________;寫出D與足量乙醇發生反應的化學方程式 。
查看答案和解析>>
科目:高中化學 來源:2016屆山東省齊魯教科研協作體19所高三上學期第一次聯考化學試卷(解析版) 題型:填空題
(6分)T℃時,向體積為2L的恒容密閉容器中充入4molA和2molB氣體,發生如下反應:4A(g)+B(g)  xC(g),保持溫度不變,5min時反應達到平衡狀態,剩余1.6 molB,并測得C的濃度為0.8mol/L,請填寫下列空白:
xC(g),保持溫度不變,5min時反應達到平衡狀態,剩余1.6 molB,并測得C的濃度為0.8mol/L,請填寫下列空白:
(1)x=__________,該反應平衡常數的表達式為:K= 。
(2)該溫度下,此反應達到平衡時,A的轉化率為α(A)= 。
(3)在T℃時,若向原平衡混合物的容器中再充入amolC,同時改變容器體積保持壓強不變,欲使達到新的平衡時,各物質的體積分數與原平衡相同,則應再充入________molB (用a表示)。
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省江南十校新高三摸底聯考化學試卷(解析版) 題型:選擇題
0.1 mol某烴完全燃燒時生成30.8 g CO2和12.6 g H2O,且能使酸性高錳酸鉀溶液褪色,若
其結構中只含有兩個一CH2,則該物質的結構(不考慮順反異構)最多有
A.6種 B.8種 C.7種 D.10種
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com