
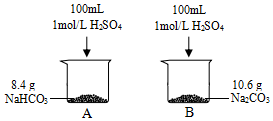
 某小組同學在實驗室研究Na2CO3與NaHCO3的性質.
某小組同學在實驗室研究Na2CO3與NaHCO3的性質.| 實驗步驟 | 實驗現象 |
| ⅰ.取1mL 0.1mol/L NaHCO3溶液,向其中加入 1mL 0.01mol/L CaCl2溶液 | 無明顯現象 |
| ⅱ.向上述溶液中滴加NaOH溶液 | 產生白色沉淀 |
分析 (1)同等條件下,碳酸鈉與硫酸反應速率不及碳酸氫鈉與硫酸反應;
(2)根據碳元素守恒可知產生氣體的體積相同;
(3)根據NaHCO3不穩定性,可將NaHCO3加熱轉變為Na2CO3;
(4)NaHCO3溶液與 Ca(OH)2溶液反應過程為:HCO3-+OH-=CO32-+H2O Ca2++CO32-=CaCO3↓;
(5)NaHCO3溶液中加入CaCl2溶液不反應,滴加NaOH溶液后,產生CaCO3沉淀.
解答 解:(1)發生反應:Na2CO3+H2SO4l═Na2SO4+H2O+CO2↑,2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑,同等條件下,碳酸鈉與硫酸反應速率不及碳酸氫鈉與硫酸反應,所以A的反應程度更為劇烈,
故答案為:>;Na2CO3與酸反應經歷兩步:CO32-+H+=HCO3-HCO3-+H+=H2O+CO2↑,而NaHCO3只有一步,因此A中產生氣體速率更快;
(2)100mL1mol/LH2SO4溶液為0.1molH2SO4,分別和8,4g(0.1mol)NaHCO3、10.6g(0.1mol)Na2CO3反應,標準狀況下,產生的CO2都為2.24L.
故答案為:=;2.24
(3)將NaHCO3加熱轉變為Na2CO3,2NaHCO3 $\frac{\underline{\;加熱\;}}{\;}$Na2CO3+H2O+CO2↑,
故答案為:2NaHCO3 $\frac{\underline{\;加熱\;}}{\;}$Na2CO3+H2O+CO2↑;
(4)NaHCO3溶液與 Ca(OH)2溶液反應過程為:HCO3-+OH-=CO32-+H2O Ca2++CO32-=CaCO3↓,
故答案為:HCO3-+OH-=CO32-+H2O; Ca2++CO32-=CaCO3↓;
(5)NaHCO3溶液中加入CaCl2溶液不反應,滴加NaOH溶液后,產生CaCO3沉淀.HCO3-+OH-=CO32-+H2O Ca2++CO32-=CaCO3↓,
故答案為:NaOH溶液; 產生白色沉淀.
點評 本題以探究碳酸氫鈉、碳酸鈉性質為載體考查物質之間反應,為高頻考點,側重于學生的分析、實驗能力的考查,注意把握物質的性質的異同.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 6Li和7Li互為同素異形體 | |
| B. | 鋰單質與氧氣反應可生成Li2O2和Li2O兩種氧化物 | |
| C. | 鋰原子在同周期主族元素中原子半徑最大 | |
| D. | 少量鋰單質保存在煤油中 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鹽酸分別與氫氧化鈉溶液、澄清石灰水反應 | |
| B. | 硫酸分別與氫氧化鈉溶液、氫氧化鋇溶液反應 | |
| C. | 硝酸分別與碳酸鈉溶液、碳酸鉀溶液反應 | |
| D. | 鋅分別與稀鹽酸、稀硫酸反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
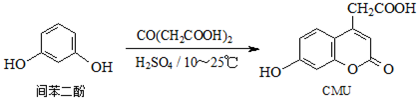
| A. | 1molCMU最多可與1molBr2反應 | |
| B. | 1molCMU最多可與3molNaOH反應 | |
| C. | 可用FeCl3溶液鑒別間苯二酚和CMU | |
| D. | CMU在酸性條件下的水解產物只有1種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18.4 mol•L-1 | B. | 34.7% | C. | 20.4 mol•L-1 | D. | 31.2% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=1的溶液:NH4+、Fe3+、CO32-、SO42- | |
| B. | 含有大量AlO2-的溶液中:Fe2+、Cu2+、Cl-、Na+ | |
| C. | 中性溶液中:Fe3+、Al3+、Na+、K+、NO3- | |
| D. | Na2S溶液中:K+、NH4+、Cl-、SO42- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com