
【題目】下列依據實驗方案和現象對濃硫酸性質做出的判斷合理的是
實驗方案 | 實驗I: | 實驗II: |
實驗現象 | 試紙中心區域變黑,邊緣變紅 | 黑色固體溶解,溶液接近無色(溶液中錳元素僅以 |
A.由I可知,濃硫酸具有脫水性B.由I可知,濃硫酸具有弱酸性
C.由II可知,濃硫酸具有強氧化性D.由II可知,濃硫酸具有吸水性
 星級口算天天練系列答案
星級口算天天練系列答案 芒果教輔達標測試卷系列答案
芒果教輔達標測試卷系列答案科目:高中化學 來源: 題型:
【題目】一定條件下,體積為10L的密閉容器中,2mol X和1mol Y進行反應:2X(g)+Y(g)![]() Z(g) ΔH<0,經20s達到平衡,生成0.5mol Z。下列說法正確的是
Z(g) ΔH<0,經20s達到平衡,生成0.5mol Z。下列說法正確的是
A.該反應平衡常數的值為1
B.將容器體積變為20L,Z的平衡濃度減小為0.025mol/L
C.以X濃度變化表示的反應速率為0.005mol/(L·s)
D.當X、Y、Z的濃度相等時,證明反應達到平衡狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D為石墨電極,E、F分別為短周期相鄰的兩種活潑金屬中的一種,且E能與NaOH溶液反應。按圖接通線路,反應一段時間,當電路中通過1.0×10-3mol電子時,下列敘述正確的是( )
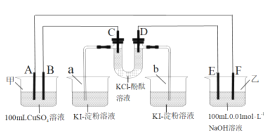
A.U型管中的D端先變紅,b燒杯中的溶液會變藍
B.a燒杯中最多有0.127gI2(KI足量)生成,甲池中的質量會減少0.04g(CuSO4溶液足量)
C.A極產生氣體的體積為5.6mL,甲池溶液的pH值為2
D.E電極附近的溶液無明顯現象產生
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學基本概念是學習化學的基石,請正確回答下列問題。
(1)今有7種物質:①液態氯化氫 ②乙醇 ③熔融的KNO3 ④銅線 ⑤NaCl晶體 ⑥小蘇打溶液 ⑦氨水。屬于電解質的是___________,屬于非電解質的是_____________。將①加入到⑦中,⑦的導電能力_______(填“增強”、“減弱”或“基本不變”)。
(2)漂白粉中加入鹽酸,可產生氯氣,化學方程式為:Ca(ClO)2+4HCl = CaCl2 +2Cl2+2H2O。用雙線橋法表示該反應中電子轉移的方向和數目_________,當有0.1 mol電子發生轉移時,生成氯氣的體積為_______L(標況下),被氧化的HCl為______mol。
(3)“四種基本反應類型與氧化還原反應的關系”如圖所示:
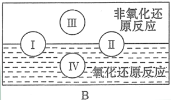
其中Ⅰ為化合反應,Ⅳ是_________反應。現有以下反應模型:單質A + 氧化物B=單質C + 氧化物D(A、B、C、D均為中學階段常見物質,反應條件已略去),寫出符合上述反應模型的化學反應方程式。
①若A為金屬單質,B為非金屬氧化物:_________________________。
②若A和C均為固體非金屬單質:_______________________________。
(4)濃硫酸有強氧化性,常溫下,向碳素鋼(僅含鐵、碳元素的合金)中加入少量濃硫酸,無明顯現象,原因是:____________________,加熱后,可能產生的氣體有___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某磁黃鐵礦的主要成分是FexS(S為-2價),既含有Fe2+又含有Fe3+。將一定量的該磁黃鐵礦與鹽酸完全反應(注:礦石中其他成分不與鹽酸反應),生成2.4 g硫單質、0.425 mol FeCl2和一定量H2S氣體,且溶液中滴加KSCN溶液不變血紅色。請計算并回答下列問題:
(1)該磁黃鐵礦FexS中,Fe2+與Fe3+的物質的量之比為_____________。
(2)該磁黃鐵礦FexS中,x=_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮的氧化物既是可導致酸雨的物質,也是造成空氣污染的重要物質,加大對氮的氧化物的治理是環境保護重要舉措。
(1)在一定條件下氨氣可用來將氮氧化物轉化為無污染的物質。寫出氨氣和二氧化氮在一定條件下反應的化學方程式: _____________________________,該反應中氧化劑是_________,還原劑是________________________________________。
(2)汽車尾氣中含有CO和NO,消除這兩種物質對大氣的污染的方法是安裝催化轉化器,使它們發生反應生成對大氣無污染的氣體,該反應的化學方程式為___________________________________。
(3)用氫氧化鈉溶液可以吸收廢氣中的氮氧化物,反應的化學方程式如下:
NO2+NO+2NaOH===2NaNO2+H2O
2NO2+2NaOH===NaNO2+NaNO3+H2O
現有VL某NaOH溶液能完全吸收nmol NO2和mmol NO組成的大氣污染物。
①所用燒堿溶液的物質的量濃度至少為_________ mol·L-1。
②若所得溶液中c(NO3-)∶c(NO2-)=1∶9,則原混合氣體中NO2和NO的物質的量之比n∶m=_________。
③用含n和m的代數式表示所得溶液中NO3-和NO2-濃度的比值c(NO3-)∶c(NO2-)=_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】考古發掘出的古代青銅器(含銅錫等金屬)表面經常出現小孔腐蝕,這是一種電化學腐蝕現象。小孔腐蝕的過程及銅腐蝕產物(銅銹)的成份如下圖所示:
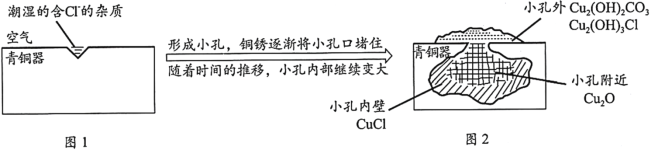
已知:2CuCl+H2O![]() Cu2O+2HCl
Cu2O+2HCl
下列分析不正確的是
A.氧氣是正極反應物B.銅銹的成份與氧氣濃度、pH有關
C.圖2中,Cl-從小孔內向小孔外移動D.青銅中的錫也會發生電化學腐蝕
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有一處于平衡狀態的可逆反應:X(s)+3Y(g)![]() 2Z(g) ΔH<0。為了使平衡向生成Z的方向移動,應選擇的條件是
2Z(g) ΔH<0。為了使平衡向生成Z的方向移動,應選擇的條件是
①高溫 ②低溫 ③高壓 ④低壓 ⑤加催化劑 ⑥分離出Z
A.①③⑤B.②③⑤C.②③⑥D.②④⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將等物質的量A、B混合于2L的密閉容器中,發生如下反應:3A(g)+ B(g)![]() xC(g)+2D(g),經5min后達到平衡,測得D的濃度為0.5mol/L,c(A)︰c(B)=3︰5,C的平均反應速率是0.1mol/(L·min)
xC(g)+2D(g),經5min后達到平衡,測得D的濃度為0.5mol/L,c(A)︰c(B)=3︰5,C的平均反應速率是0.1mol/(L·min)
請計算:(寫出計算過程,無過程不給分)
(1)平衡時A的濃度;______反應開始前容器中B的物質的量;_____
(2)前5 min內用B表示的平均反應速率;______
(3)化學反應方程式中x的值;_____
(4)5min時物質A的轉化率。____
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com