
 (1)20世紀30年代,Eyring和Pzer在碰撞理論的基礎上提出化學反應的過渡態理論:化學反應并不是通過簡單的碰撞就能完成的,而是在反應物到生成物的過程中經過一個高能量的過渡態.如圖是NO2和CO反應生成CO2和NO過程中的能量變化示意圖,說明這個反應是
(1)20世紀30年代,Eyring和Pzer在碰撞理論的基礎上提出化學反應的過渡態理論:化學反應并不是通過簡單的碰撞就能完成的,而是在反應物到生成物的過程中經過一個高能量的過渡態.如圖是NO2和CO反應生成CO2和NO過程中的能量變化示意圖,說明這個反應是 CO2+NO,2min時,測得容器中NO的物質的量為0.2mol,則:
CO2+NO,2min時,測得容器中NO的物質的量為0.2mol,則:| △c |
| t |
| m |
| n |
 CO2 +NO,
CO2 +NO,| △c |
| t |
| 0.1mol/L |
| 2min |
| m |
| n |


 步步高達標卷系列答案
步步高達標卷系列答案科目:高中化學 來源: 題型:閱讀理解



| 化學鍵 | P-P | P-O | O=O | P=O |
| 鍵能/kJ?mol-1 | 197 | 360 | 499 | X |
查看答案和解析>>
科目:高中化學 來源: 題型:
A.CH3SH B.CH3CH2SH
C.(CH3)2CHSH D.CH3CH2CH2CH2SH
查看答案和解析>>
科目:高中化學 來源: 題型:

圖Ⅰ
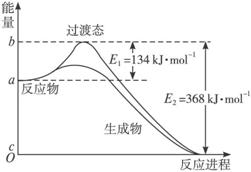
圖Ⅱ
(1)圖Ⅰ是HI分解反應中HI分子之間的幾種碰撞示意圖,其中屬于有效碰撞的是_______(選填“A”“B”或“C”)。
(2)20世紀30年代,Eyring和Pelzer在碰撞理論的基礎上提出化學反應的過渡態理論:化學反應并不是通過簡單的碰撞就能完成的,而是在反應物到生成物的過程中經過一個高能量的過渡態。
圖Ⅱ是NO2和CO反應生成CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式:___________________________。
(3)過渡態理論認為,催化劑改變反應速率的原因是改變了反應的途徑,對大多數反應而言主要是通過改變過渡態而導致有效碰撞所需要的能量發生變化。請在圖Ⅱ中作出NO2和CO反應時使用催化劑而使反應速率加快的能量變化示意圖。
(4)進一步研究表明,化學反應的能量變化(ΔH)與反應物和生成物的鍵能有關。鍵能可以簡單地理解為斷開1 mol化學鍵時所需吸收的能量。下表是部分化學鍵的鍵能數據:
化學鍵 | P—P | P—O | O=O | P=O |
鍵能/kJ·mol-1 | 197 | 360 | 499 | X |

圖Ⅲ
已知白磷的燃燒熱為2 378.0 kJ·mol-1,白磷完全燃燒的產物結構如圖Ⅲ所示,則上表中X=_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
(7分)1918年,Lewis提出反應速率的碰撞理論:反應物分子間的相互碰撞是反應進行的必要條件,但并不是每次碰撞都能引起反應,只有少數碰撞才能發生化學反應。能引發化學反應的碰撞稱之為有效碰撞。
(1)圖I是HI分解反應中HI分子之間的幾種碰撞示意圖,其中屬于有效碰撞的是 (選填“A”、“B”或“C”);
(2)20世紀30年代,Eyring和Pelzer在碰撞理論的基礎上提出化學反應的過渡態理論:化學反應并不是通過簡單的碰撞就能完成的,而是在反應物到生成物的過程中經過一個高能量的過渡態。圖Ⅱ是NO2和CO反應生成CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式:
(3) 過渡態理論認為,催化劑改變反應速率的原因是改變了反應的途徑,對大多數反應而言主要是通過改變過渡態而導致有效碰撞所需要的能量發生變化。請在圖Ⅱ中作出NO2和CO反應時使用催化劑而使反應速率加快的能量變化示意圖;
查看答案和解析>>
科目:高中化學 來源:2013屆浙江寧波金蘭合作組織高二下學期期中聯考化學試卷(解析版) 題型:填空題
(10分)1918年,Lewis提出反應速率的碰撞理論:反應物分子間的相互碰撞是反應進行的必要條件,但并不是每次碰撞都能引起反應,只有少數碰撞才能發生化學反應。能引發化學反應的碰撞稱之為有效碰撞。
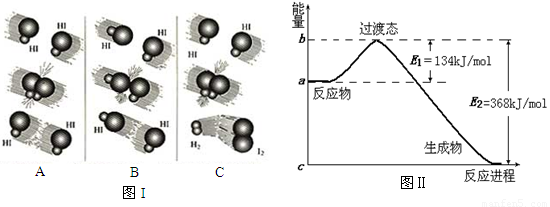
(1)圖I是HI分解反應中HI分子之間的幾種碰撞示意圖,其中屬于有效碰撞的是 (選填“A”、“B”或“C”);
(2)20世紀30年代,Eyring和Pelzer在碰撞理論的基礎上提出化學反應的過渡態理論:化學反應并不是通過簡單的碰撞就能完成的,而是在反應物到生成物的過程中經過一個高能量的過渡態。圖Ⅱ是NO2和CO反應生成CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式: ;(圖中為1molNO2與1molCO的反應)
(3)過渡態理論認為,催化劑改變反應速率的原因是改變了反應的途徑,對大多數反應而言主要是通過改變過渡態而導致有效碰撞所需要的能量發生變化。
①在體系中加入催化劑對反應熱是否有影響? (填“是”或“否”),原因是 。
②在反應體系中加入催化劑,反應速率增大,E1和E2的變化是:E1 ,E2 。(填“增大”、“減小”或“不變”)
③請在圖Ⅱ中作出NO2和CO反應時使用催化劑而使反應速率加快的能量變化示意圖:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com