
二氧化硒(SeO2)是一種氧化劑,其被還原后的單質硒可能成為環境污染物,通過與濃HNO3或濃H2SO4反應生成SeO2以回收Se。完成下列填空:
(1)Se和濃HNO3反應的還原產物為NO和NO2,且NO和NO2的物質的量之比為1∶1,寫出Se和濃HNO3的反應方程式___________________________________________。
(2)已知:Se+2H2SO4(濃)―→2SO2↑+SeO2+2H2O,2SO2+SeO2+2H2O―→Se+2SO42—+4H+,則SeO2、H2SO4(濃)、SO2的氧化性由強到弱的順序是______________。
(3)回收得到的SeO2的含量,可以通過下面的方法測定: ①SeO2+KI+HNO3―→Se+I2+KNO3+H2O
②I2+2Na2S2O3―→Na2S4O6+2NaI。配平方程式①,標出電子轉移的方向和數目。
(4)實驗中,準確稱量SeO2樣品0.150 0 g,消耗了0.200 0 mol/L的Na2S2O3溶液25.00 mL,所測定的樣品中SeO2的質量分數為________。
(1)Se+2HNO3(濃)―→H2SeO3+NO↑+NO2↑ (2)H2SO4(濃)>SeO2>SO2?
(3) 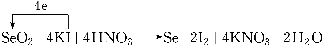
(4)0.925
【解析】利用題中信息可知Se與濃HNO3反應,Se被氧化為+4價的H2SeO3,HNO3還原為NO與NO2,利用電子守恒和限定條件(生成NO與NO2的物質的量之比為1∶1,即二者計量系數比為1∶1)可得方程式。利用氧化性:氧化劑>氧化產物,結合題中方程式可知氧化性:H2SO4(濃)>SeO2>SO2。在反應①中I-失去電子,+4價Se得到電子被還原為單質Se。利用前面配平的方程式可得關系式:SeO2~2I2~4Na2S2O3,故樣品中SeO2的質量分數為:
[111 g·mol-1×(0.200 0 mol/L×0.025 L)/4]/0.150 0 g=0.925。


科目:高中化學 來源: 題型:
二氧化硒(SeO2)是一種氧化劑,其被還原后的單質硒可能成為環境污染物,通過與濃HNO3或濃H2SO4反應生成SeO2以回收Se。
完成下列填空:
27.Se和濃HNO3反應的還原產物為NO和NO2,且NO和NO2的物質的量之比為1:1,寫出Se和濃HNO3的反應方程式________。
28.已知:Se+2H2SO4(濃)→2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O→Se+2SO42-+4H+
SeO2、H2SO4(濃)、SO2的氧化性由強到弱的順序是______。
29.回收得到的SeO2的含量,可以通過下面的方法測定:
①SeO2+KI+HNO3→Se+I2+KNO3+H2O
②I2+2Na2S2O3→Na2S4O6+2NaI
配平方程式①,標出電子轉移的方向和數目。
30.實驗中,準確稱量SeO2樣品0.1500g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所測定的樣品中SeO2的質量分數為___。
查看答案和解析>>
科目:高中化學 來源:2013屆福建省三明市泰寧一中高三第二次月考化學試卷(帶解析) 題型:填空題
(5分)二氧化硒(SeO2)是一種氧化劑,其被還原后的單質硒可能成為環境污染物,通過與濃HNO3或濃H2SO4反應生成SeO2以回收Se。完成下列填空:
(1)Se和濃HNO3反應的還原產物為NO和NO2,且NO和NO2的物質的量之比為1:1,寫出Se和濃HNO3的反應方程式____ ____。
(2)已知:Se+2H2SO4(濃)→2SO2↑+SeO2+2H2O ; 2SO2+SeO2+2H2O→Se+2SO42-+4H+
則SeO2、H2SO4(濃)、SO2的氧化性由強到弱的順序是____ __。
(3)回收得到的SeO2的含量,可以通過下面的方法測定,測定的原理如下:反應①發生后產生的I2,I2的量在反應②中被滴定,淀粉為指示劑,以Na2S2O3溶液為標準溶液
①SeO2+KI+HNO3→Se+I2+KNO3+H2O
②I2+2Na2S2O3→Na2S4O6+2NaI
實驗中,準確稱量SeO2樣品0.2500g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所測定的樣品中SeO2的質量分數為_ __。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年貴州省高三第二次月考理科綜合化學試卷(解析版) 題型:選擇題
鳳崗的“富鋅富硒”茶現已享譽全國,富含硒元素,有延年益壽、抗衰老等作用。二氧化硒(SeO2)是一種氧化劑,其被還原后的單質硒可能成為環境污染物,通過與濃HNO3、濃H2SO4反應生成SeO2以回收Se。在回收過程當中涉及到如下兩個化學反應①SeO2+4KI+4HNO3= Se+2I2+4KNO3+2H2O;② Se+2H2SO4(濃) ==2SO2↑+SeO2+2H2O,下列有關敘述正確的是
A.SeO2、H2SO4(濃)、I2的氧化性由強到弱的順序是H2SO4(濃)> SeO2> I2。
B.①中Se是氧化產物,I2是還原產物
C.反應①中KI是氧化劑,SeO2是還原劑
D.反應①中每有1.0 mol I2生成,轉移電子數目為4NA
查看答案和解析>>
科目:高中化學 來源:2012-2013學年福建省三明市高三第二次月考化學試卷(解析版) 題型:填空題
(5分)二氧化硒(SeO2)是一種氧化劑,其被還原后的單質硒可能成為環境污染物,通過與濃HNO3或濃H2SO4反應生成SeO2以回收Se。完成下列填空:
(1)Se和濃HNO3反應的還原產物為NO和NO2,且NO和NO2的物質的量之比為1:1,寫出Se和濃HNO3的反應方程式____ ____。
(2)已知:Se+2H2SO4(濃)→2SO2↑+SeO2+2H2O ; 2SO2+SeO2+2H2O→Se+2SO42-+4H+
則SeO2、H2SO4(濃)、SO2的氧化性由強到弱的順序是____ __。
(3)回收得到的SeO2的含量,可以通過下面的方法測定,測定的原理如下:反應①發生后產生的I2,I2的量在反應②中被滴定,淀粉為指示劑,以Na2S2O3溶液為標準溶液
①SeO2+KI+HNO3→Se+I2+KNO3+H2O
②I2+2Na2S2O3→Na2S4O6+2NaI
實驗中,準確稱量SeO2樣品0.2500g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所測定的樣品中SeO2的質量分數為_ __。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com