
| A. | 硫原子的原子結構示意圖: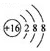 | |
| B. | 原子核內有10個質子的氧原子${\;}_{8}^{18}$O | |
| C. | NH4Cl的電子式: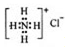 | |
| D. | 鄰氯甲苯的結構簡式: |
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 研究表明豐富的CO2完全可以作為新碳源,解決當前應用最廣泛的碳源(石油和天然氣)到本世紀中葉將枯竭的危機,同時又可緩解由CO2累積所產生的溫室效應,實現CO2的良性循環.
研究表明豐富的CO2完全可以作為新碳源,解決當前應用最廣泛的碳源(石油和天然氣)到本世紀中葉將枯竭的危機,同時又可緩解由CO2累積所產生的溫室效應,實現CO2的良性循環.| 實驗組 | 溫度℃ | 起始量/mol | 平衡量/mol | 達到平衡所需 時間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
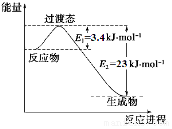
 已知有關熱化學方程式為:①4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g)2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反應①中有關化學鍵的鍵能(kJ/mol)如下:H-O:463,H-N:391,O=O:497
已知有關熱化學方程式為:①4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g)2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反應①中有關化學鍵的鍵能(kJ/mol)如下:H-O:463,H-N:391,O=O:497查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
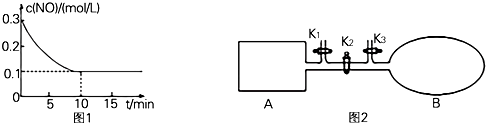
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 比較非金屬性強弱:Si弱于C,C弱于S | |
| B. | 用四氯化碳提取碘水中的碘單質 | |
| C. | 觀察燒堿的焰色反應 | |
| D. | 比較NaHCO3和Na2CO3的熱穩定性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧燃料電池在堿性介質中的負極反應式:O2+2H2O+4e-=4OH- | |
| B. | 電解飽和食鹽水時,陽極的電極反應式為:2Cl--2e-=Cl2↑ | |
| C. | 粗銅精煉時,與電源正極相連的是純銅,電極反應式為:Cu-2e-=Cu2+ | |
| D. | 鋼鐵發生電化學腐蝕的正極反應式:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com