
| A. | 可逆反應的特征是正反應速率和逆反應速率相等 | |
| B. | 在其他條件不變時,使用催化劑只能改變反應速率,而不能改變化學平衡狀態 | |
| C. | 在其他條件不變時,升高溫度可以使平衡向正反應方向移動 | |
| D. | 對于反應A(g)+3B(g)?2C(g)△H<0達平衡后,溫度降低,正反應速率增大,逆反應速率減小,平衡向正反應方向移動 |
分析 A.可逆反應為在相同條件下正反應和逆反應同時進行的反應,化學平衡狀態的本質特征為同種物質的生成速率與消耗速率相等;
B.使用催化劑可以改變化學反應速率,但不能改變化學平衡狀態;
C.升高溫度可以使化學平衡向吸熱反應的方向移動;
D.降低溫度,正、逆反應速率都減小.
解答 解:A.可逆反應為在相同條件下正反應和逆反應同時進行的反應,正、逆反應速率相等為化學平衡狀態的特征,不是可逆反應的特征,故A錯誤;
B.使用催化劑可以改變化學反應速率,但不能改變化學平衡狀態,故B正確;
C.升高溫度可以使化學平衡向吸熱反應的方向移動,由于反應是吸熱還是放熱未知,不能確定平衡移動方向,故C錯誤;
D.降低溫度,正、逆反應速率都減小,正反應為放熱反應,平衡正向移動,正反應速率降低更少,故D錯誤,
故選:B.
點評 本題考查可逆反應、化學平衡狀態特征、化學平衡影響因素、反應速率影響因素,理解掌握改變條件反應速率變化與平衡移動關系.


 全能測控一本好卷系列答案
全能測控一本好卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 氯化鈉水溶液在電流的作用下電離出Na+和Cl- | |
| B. | 二氧化碳的水溶液能夠導電,故二氧化碳屬于電解質 | |
| C. | 碳酸氫鈉在水中電離的離子方程式為NaHCO3═Na++H++CO32- | |
| D. | 碳酸鈉屬于電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 元素A的一種單質是太陽能電池中的主要材料 | |
| B. | 元素C的某單質與過氧化鈉的漂白原理類似 | |
| C. | B和E可組成一種耐高溫的結構材料,其化學式為E4B3 | |
| D. | 工業上制取E單質時,生成的氣體主要是AO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
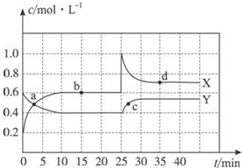 已知NO2和N2O4可以相互轉化:2NO2(g)?N2O4(g)△H<0.現將一定量NO2和N2O4的混合氣體通入一定體積為2L的恒溫密閉玻璃容器中,反應物濃度隨時間變化關系如圖.
已知NO2和N2O4可以相互轉化:2NO2(g)?N2O4(g)△H<0.現將一定量NO2和N2O4的混合氣體通入一定體積為2L的恒溫密閉玻璃容器中,反應物濃度隨時間變化關系如圖.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電解飽和食鹽水制取氫氣 | |
| B. | 大量設立水電站,用電力分解水制取氫氣. | |
| C. | 設法將太陽能聚焦,產生高溫,使水分解產生氫氣. | |
| D. | 尋找更多的化石燃料,利用其燃燒放熱,使水分解產生氫氣. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,11.2L的戊烷含有分子數為0.5NA | |
| B. | 常溫下,14g乙烯和丙烯的混合物中總原子數為3NA | |
| C. | 1mol甘氨酸(α-氨基乙酸)分子中存在9NA對共用電子 | |
| D. | 1L0.1mol/L的苯酚分子數為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 相同條件下,硅甲烷的密度小于甲烷 | |
| B. | 硅甲烷燃燒生成二氧化硅和水 | |
| C. | 硅烷的分子通式可表示為SinH2n+2 | |
| D. | 硅甲烷與硅乙烷的相對分子質量相差30 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com