
| A. | Fe與Cl2反應生成FeCl3,推測Fe與I2反應生成FeI3 | |
| B. | SiH4的沸點高于CH4,推測H2S的沸點高于H2O | |
| C. | CO2是直線型分子,推測CS2也是直線型分子 | |
| D. | NaCl與濃H2SO4加熱可制HCl,推測NaBr與濃H2SO4加熱可制HBr |
分析 A.I2的氧化性較弱,碘單質與鐵反應生成FeI2;
B.C和Si,O和S都分別同族元素,形成的氫化物都為分子晶體,沸點取決于分子間作用力的大小;
C.O和S同主族,二者形成的CO2和CS2都是直線形分子;
D.濃硫酸能夠將HBr氧化為Br2.
解答 解:A.因I2的氧化性較弱,在碘單質與鐵反應生成的是FeI2,故A錯誤;
B.C和Si,O和S都分別為同族元素,所形成的氫化物都為分子晶體,而水分子間存在氫鍵,所以沸點異常的高,則H2O沸點高于H2S,故B錯誤;
C.O和S是同族元素,故形成的CO2和CS2都是直線形分子,該推理合理,故C正確;
D.濃硫酸氧化性很強,能夠將HBr氧化為Br2,不能用該方法制取HBr,故D錯誤;
故選C.
點評 本題考查較為綜合,涉及分子構型、晶體性質、鐵的化學性質、濃硫酸的性質等知識,題目難度中等,明確常見元素及其化合物性質為解答關鍵,試題培養了學生的分析能力及靈活應用能力.


 A加金題 系列答案
A加金題 系列答案 全優測試卷系列答案
全優測試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 向硫酸亞鐵溶液中加入雙氧水的離子方程式:Fe2++2H2O+4H+=Fe3++4H2O | |
| B. | 粗硅制備的化學方程式:C+SiO2$\frac{\underline{\;高溫\;}}{\;}$CO2↑+Si | |
| C. | 石墨作電極電解CuSO4溶液的離子方程式:2Cu2++2H2O$\frac{\underline{\;電解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 鐵發生吸氧腐蝕時負極上的電極反應式:Fe-3e-=Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
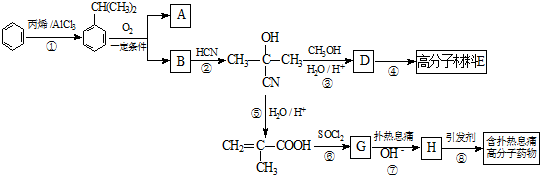
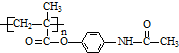 .
.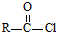
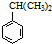 可轉化為1mol A和1mol B,且A與FeCl3溶液作用顯紫色,寫出A的稀溶液與過量濃溴水發生反應的化學方程式
可轉化為1mol A和1mol B,且A與FeCl3溶液作用顯紫色,寫出A的稀溶液與過量濃溴水發生反應的化學方程式

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 為探究亞硫酸鈉的熱穩定性,某研究性學習小組將無水亞硫酸鈉隔絕空氣加熱,并利用受熱后的固體試樣和下圖所示的實驗裝置進行實驗.請回答下列有關問題:
為探究亞硫酸鈉的熱穩定性,某研究性學習小組將無水亞硫酸鈉隔絕空氣加熱,并利用受熱后的固體試樣和下圖所示的實驗裝置進行實驗.請回答下列有關問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C3H8,C4H6 | B. | C3H6,C4H6O2 | C. | C2H2,C6H6 | D. | CH4O,C2H4O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
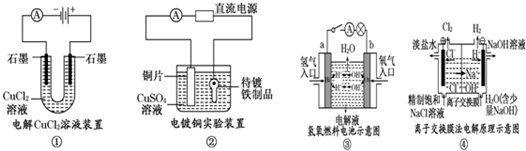
| A. | 裝置①中陽極上析出紅色固體 | |
| B. | 裝置②的待鍍鐵制品應與電源負極相連 | |
| C. | 裝置③中外電路電子由a極流向b極 | |
| D. | 裝置④的陽極反應為:2H++2e-=H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 23g金屬鈉變為鈉離子時失電子數目為1 NA | |
| B. | 18g水所含有的電子數為NA | |
| C. | 4克氫氣所含的分子數為NA | |
| D. | 4gCH4所含有的氫原子數目為2NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com