
 某校化學興趣小組為探究FeSO4和NaHCO3的反應,按如圖所示操作將NaHCO3溶液滴加到FeSO4溶液中(FeSO4和NaHCO3溶液均用經煮沸后冷卻的蒸餾水配制,并在FeSO4溶液中加入少量鐵粉).觀察到試管中立即出現白色沉淀,同時有大量無色氣體生成.
某校化學興趣小組為探究FeSO4和NaHCO3的反應,按如圖所示操作將NaHCO3溶液滴加到FeSO4溶液中(FeSO4和NaHCO3溶液均用經煮沸后冷卻的蒸餾水配制,并在FeSO4溶液中加入少量鐵粉).觀察到試管中立即出現白色沉淀,同時有大量無色氣體生成.分析 (1)配制10%的NaHCO3溶液,需要用托盤天平量取碳酸氫鈉的質量,還需要用量筒量取水的體積;
(2)亞鐵離子和碳酸氫根離子發生雙水解反應生成CO2;
(3)白色固體可能是Fe(OH)2和FeCO3的混合物;
(4)FeSO4和NaHCO3反應生成Fe(OH)2沉淀、二氧化碳和硫酸鈉;二價鐵不穩定,易被氧氣氧化而干擾實驗;堿性條件下,亞鐵離子生成Fe(OH)2沉淀;
(5)如果白色沉淀是Fe(OH)2,Fe(OH)2不穩定,極易被氧化生成Fe(OH)3;FeCO3在干燥空氣中穩定,潮濕環境中需較長時間才能被氧化為Fe(OH)3,通入空氣后根據白色固體變色時間長短判斷白色沉淀成分.
解答 解:(1)實驗室欲配制10%的NaHCO3溶液,所需儀器有:燒杯、玻璃棒、藥匙,還缺少稱量碳酸氫鈉質量的儀器托盤天平及量取水的體積的儀器量筒,
故答案為:托盤天平;量筒;
(2)亞鐵離子和碳酸氫根離子發生雙水解反應生成氫氧化亞鐵和CO2,所以生成的氣體是CO2,故答案為:CO2;
(3)白色固體可能是Fe(OH)2和FeCO3的混合物,所以假設3為白色固體是Fe(OH)2和FeCO3,故答案為:Fe(OH)2和FeCO3;
(4)FeSO4和NaHCO3反應生成Fe(OH)2沉淀、二氧化碳,根據元素守恒知還生成硫酸鈉,反應方程式為FeSO4+2NaHCO3=Fe(OH)2↓+Na2SO4+2CO2↑;
二價鐵不穩定,易被氧氣氧化而干擾實驗,所以經煮沸后冷卻的蒸餾水配制FeSO4和NaHCO3溶液的目的是除去水中溶解的氧氣,防止生成的氫氧化亞鐵被迅速氧化;
反應體系進行了無氧處理并且碳酸氫鈉水解提供了堿性環境,所以白色沉淀中一定含有氫氧化亞鐵,
故答案為:FeSO4+2NaHCO3=Fe(OH)2↓+Na2SO4+2CO2↑;除去水中溶解的氧氣,防止生成的氫氧化亞鐵被迅速氧化;不同意;
(5)如果白色沉淀是Fe(OH)2,Fe(OH)2不穩定,極易被氧化生成Fe(OH)3;FeCO3在干燥空氣中穩定,潮濕環境中需較長時間才能被氧化為Fe(OH)3,通入空氣后根據白色固體變色時間長短判斷白色沉淀成分,所以其實驗步驟、預期現象和結論為:向生成的白色沉淀的試管中通入空氣,若白色沉淀迅速變成灰綠色,最后變為紅褐色,則假設2不成立;若白色沉淀短時間內不變色,則假設2成立,
故答案為:向生成的白色沉淀的試管中通入空氣,若白色沉淀迅速變成灰綠色,最后變為紅褐色,則假設2不成立;若白色沉淀短時間內不變色,則假設2成立.
點評 本題考查性質實驗方案設計,題目難度中等,側重考查學生分析、判斷及實驗操作能力,明確實驗原理及物質性質是解本題關鍵,難點是(5)實驗方案設計方法,需要利用物質性質的不同點設計方案.


科目:高中化學 來源: 題型:多選題
| A. | 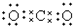 | B. | K+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$H]- | ||
| C. | 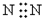 | D. |  |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | C2H6 | B. | C4H8 | C. | C3H8 | D. | C3H6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | a=b+m-n | B. | a=b-m+n | C. | a-m=b+n | D. | a-m=b-n |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Li、Na同主族,因為Na在空氣中加熱生成Na2O2,所以Li在空氣中加熱生成Li2O2 | |
| B. | F、Cl同主族,因為HCl是強酸,所以HF也是強酸 | |
| C. | Li、Na同主族,因為Na保存在煤油中,所以Li也保存在煤油中 | |
| D. | F、Cl同主族,因為Cl2也是有色氣體,所以F2也是有色氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ns2 | B. | ns2np1 | C. | ns2np4 | D. | ns2np5 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
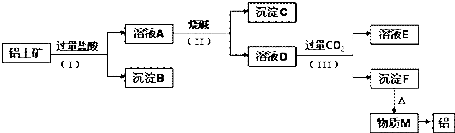
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 序號、物理量 | M(Fe粉)/g | V[0.05mol.L-1Na2S2O8]/mL | V[H2O]/mL | 收集數據和得出結論 | |
| 1 | 100 | 0.3 | 50 | 50 | |
| 2 | 100V(污水)/mL | 0.3 |
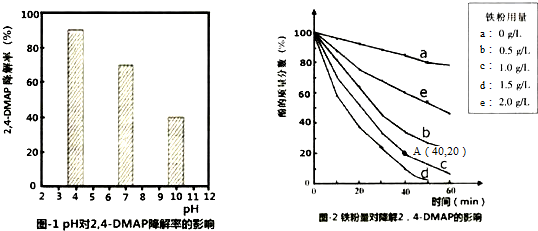
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
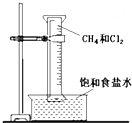 如圖所示,用排飽和食鹽水法先后收集20ml CH4和 80mlCl2,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,觀察發生的現象.回答下列問題:
如圖所示,用排飽和食鹽水法先后收集20ml CH4和 80mlCl2,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,觀察發生的現象.回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com